
| 化学键 | Cl-Cl | Br-Br | I-I | H-Cl | H-Br | H-I | H-H |
| 键能(kJ/mol) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
分析 (1)物质中的化学键键能越大,断裂时吸收的热量越多,则化学键越稳定;
(2)X2+H2═2HX,依据键能数据分析氯气和氢气反应生成氯化氢反应,溴单质和氢气反应生成溴化氢的反应,碘单质和氢气反应生成碘化氢反应都是放热反应;
(3)相同条件下,等物质的量的X2(卤素单质)分别与足量的氢气反应,依据键能计算分析判断.
解答 解:(1)根据表格中的数据可知,物质中H-H键能最大,断裂时吸收的能量越多,越难以断裂,所以H-H最稳定;
故选A;
(2)X2+H2═2HX,反应焓变=反应物总键能-生成物总键能,
H2+Cl2=2HCl△H=243kJ/mol+436kJ/mol-432kJ/mol×2=-185kJ/mol,
H2+Br2=2HBr△H=193kJ/mol+436kJ/mol-2×366kJ/mol=-103kJ/mol
I2+H2=2HI△H=151kJ/mol+436kJ/mol-2×298kJ/mol=-9kJ/mol;
所以X2+H2═2HX(X代表卤族原子)的反应是放热反应;
故答案为:放热;
(3)通过上述计算可知,相同条件下,等物质的量的X2(卤素单质)分别与足量的氢气反应,非金属性越强放出热量最多的是F2,故答案为:F2.
点评 本题考查了反应能量变化分析判断,主要是根据键能计算反应焓变的应用,掌握基础是关键,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
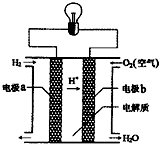
| A. | a电极是负极 | |
| B. | 该电池的总反应:2H2+O2═2H2O | |
| C. | 产物为无污染的水,属于环境友好电池 | |
| D. | 外电路中电子b电极通过导线流向a电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 条件 | |
| 温度/℃ | 催化剂 | |
| 1 | 40 | FeCl3溶液 |
| 2 | 20 | FeCl3溶液 |
| 3 | 20 | MnO2 |
| 4 | 20 | 无 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
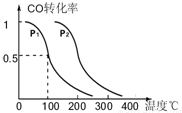
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式可以表示为CH2CH2 | |
| B. | 苯、乙醇和乙酸都能发生取代反应 | |
| C. | 糖类、油脂、蛋白质均为高分子化合物 | |
| D. | 乙酸不能与NaHCO3溶液反应生成CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )| A. | 原子半径:X<Z<W | |
| B. | 气态氢化物的稳定性:X>Y | |
| C. | 非金属性:Z>Y | |
| D. | 最高价氧化物对应水化物的酸性:W>Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com