
化学与生产、生活密切相关,下列叙述错误的是( )·
A.用热的的纯碱溶液清除灶具上的油污
B.用硫酸清洗锅炉中的水垢
C.用明矾[KAl(SO4)2 ·12H2O]作净水剂,除去水中悬浮的杂质
D.用Na2S作沉淀剂,除去废水中的Cu2+和Hg2+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期末化学卷(解析版) 题型:选择题
下列说法中正确的是( )
A.同温同压下,具有相同数目分子的气体必具有相同的体积
B.等质量的O2和H2的物质的量之比为16∶1
C.不同的气体若体积不等,则它们所含的分子数一定不等
D.同温同体积下,两种气体的物质的量之比等于密度之比
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三模拟四化学卷(解析版) 题型:选择题
继屠呦呦从青蒿中成功提取出青蒿素后,中国科学院上海有机化学研究所又在1982年人工合成了青蒿素,其部分合成路线如下所示:

下列说法不正确的是:
A. 香茅醛存在顺反异构现象
B. “甲→乙”发生了取代反应
C. 甲中不同化学环境的羟基都能发生催化氧化反应
D. 香茅醛能发生加聚反应和缩聚反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上期中化学卷(解析版) 题型:选择题
已知常温下:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,下列叙述正确的是( )
A. AgCl在饱和NaCl溶液中的KSP比在纯水中的KSP小
B. 向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明KSP(AgCl)<KSP(AgBr)
C. 将0.001mol•L-1 AgNO3溶液滴入0.001mol•L-1 KCl和0.001mol•L-1 K2CrO4混合溶液中,先产生Ag2CrO4沉淀
D. 向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上期中化学卷(解析版) 题型:选择题
25℃时,在饱和氯水中存在平衡:Cl2+H2O H++Cl-+HClO,下列叙述中正确的是( )
H++Cl-+HClO,下列叙述中正确的是( )
A.用pH试纸测得溶液pH<7
B.向其中加入AgNO3溶液,平衡向右移,溶液的pH变小
C.向其中加入NaOH使pH=7,所得溶液中微粒浓度的关系如下:c(Na+)>c(Cl-)>c(ClO-)=c(HClO)
D.若氯水久置pH会逐渐增大
查看答案和解析>>
科目:高中化学 来源:2017届天津市高三上月考三化学试卷(解析版) 题型:选择题
对于密闭容器中可逆反应 A2(g)+3B2(g) 2AB3(g),探究单一条件改变情况下,可能引起平衡状态的改变,得到如下图所示的曲线(图中T表示温度,n 表示物质的量)下列判断正确的是( )
2AB3(g),探究单一条件改变情况下,可能引起平衡状态的改变,得到如下图所示的曲线(图中T表示温度,n 表示物质的量)下列判断正确的是( )
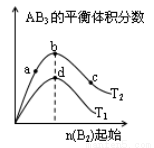
A.加入催化剂可以使状态 d 变为状态 b
B.若 T1>T2,则逆反应一定是放热反应
C.达到平衡时 A2 的转化率大小为: b>a>c
D.在T2 和n(A2)不变时达到平衡,AB3 的物质的量大小为: c>b>a
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上月考五化学试卷(解析版) 题型:填空题
【化学——选修物质结 构与性质】主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
构与性质】主族元素碳、氧、氮、氟、磷、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
(1)在基态14C原子中,核外存在 对自旋相反的电子,基态氮原子的价层电子排布图为_________________________。
(2)将F2通入稀NaOH溶液中可生成OF2,OF2分子构型为 ,其中氧原子的杂化方式为 。
(3)过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n= 。CO与N2结构相似,CO分子内σ键与π键个数之比为 。
(4)CuSO4溶液能用作P4中毒的解毒剂,反应可生成P的最高价含氧酸和铜,该反应的化学方程式是 。
(5)H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系解释H2SeO4比H2SeO3酸性强的原因: ;
(6)已知Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有 个铜原子。
(7)用晶体的X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为面心立方最密堆积(如右图),已知该晶体的密度为9.00 g·cm-3,Cu的原子半径为________cm(阿伏加德罗常数为NA,只要求列式表示)。

查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上月考二化学卷(解析版) 题型:选择题
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
A.脱氧过程是吸热反应,可降低温度,延长糕点保质期
B.脱氧过程中铁作原电池正极,电极反应为:Fe-3e→Fe3+
C.脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e→4OH-
D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上期末文化学卷(解析版) 题型:选择题
分散质粒子直径在1nm~100nm 之间的分散系是
A、溶液 B、乳浊液 C、胶体 D、悬浊液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com