
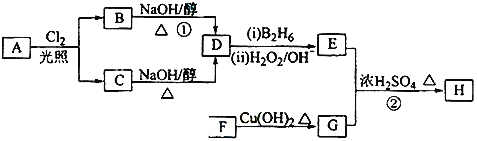
����Ŀ��������H��������·�ߺϳɣ�
��֪��![]()
�ش��������⣺
��1��11.2L����״��������A�������г��ȼ�տ�������88g CO2��45g H2O����A���ӽṹ����3��������A�Ľṹ��ʽΪ______________��
��2��B��C��Ϊһ�ȴ�����D�����ƣ�ϵͳ������Ϊ_______________��
��3���ڴ���������1mol F��2mol H2��Ӧ������3��������1��������F�Ľṹ��ʽ ��_________________________________________________________________________��
��4����Ӧ�ٵķ�Ӧ������_________________________________________________________��
��5����Ӧ�ڵĻ�ѧ����ʽΪ______________________________________________________��
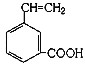
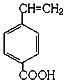
��6��д����G������ͬ�����ŵķ������G��ͬ���칹��Ľṹ��ʽ___________________��(��дһ�֡���
���𰸡���CH3��3CH2������ϩ![]() ��ȥ��Ӧ
��ȥ��Ӧ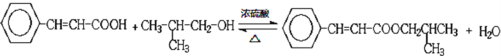
 ��
�� ��
�� ��
��![]() ����
����
��������
88gCO2�����ʵ���Ϊ��88g��44g/mol=2mol��45gH2O�����ʵ���Ϊ��45g��18g/mol=2.5mol�������11.2L��AΪ�����ʵ���Ϊ��11.2L��22.4L/mol=0.5mol��������A�к�̼ԭ����Ϊ4��Hԭ����Ϊ10����A�Ļ�ѧʽΪC4H10��A�к���3��������AΪ��CH3��3CH��A��Cl2���������·���һ��ȡ��ʱ�����ֲ��2-��-1-�ȱ����2-��-2-�ȱ��飬��NaOH����Һ�����·�����ȥ��Ӧ����DΪCH2=C(CH3)2��D������Ϣ�еķ�Ӧ����EΪ![]() ��F����Cu(OH)2��Ӧ��˵��F�к���ȩ����1mol F��2mol H2��Ӧ����3-����-1-����������̼̼˫������F�Ľṹ��ʽΪ
��F����Cu(OH)2��Ӧ��˵��F�к���ȩ����1mol F��2mol H2��Ӧ����3-����-1-����������̼̼˫������F�Ľṹ��ʽΪ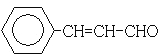 ��F��ȩ������Ϊ�Ȼ�����GΪ
��F��ȩ������Ϊ�Ȼ�����GΪ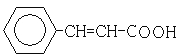 ��G��E����������Ӧ����HΪ
��G��E����������Ӧ����HΪ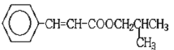 ��
��
��1��.���ݷ�����֪��A�Ľṹ��ʽΪ��CH3��3CH���ʴ�Ϊ����CH3��3CH��
��2��.D�Ľṹ��ʽΪCH2=C(CH3)2�����л��������Ϊ2-����ϩ���ʴ�Ϊ��2-����ϩ��
��3��.������������֪��F�Ľṹ��ʽΪ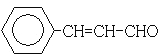 ���ʴ�Ϊ��
���ʴ�Ϊ��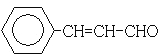 ��
��
��4��. ��Ӧ��Ϊ±������NaOH����Һ�м��ȷ�����ȥ��Ӧ���ʴ�Ϊ����ȥ��Ӧ��
��5��.��Ӧ��Ϊ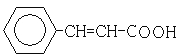 ��
��![]() ����������Ӧ����
����������Ӧ����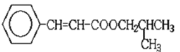 ��ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ��
��ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ��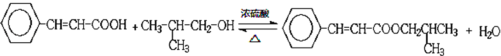 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��6��.GΪ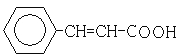 �����еĹ�����Ϊ̼̼˫�����Ȼ���������ͬ�����ŵķ������G��ͬ���칹�壬���Խ������ű任��Ӧ��λ�õó��䷼�����ͬ���칹�壬��
�����еĹ�����Ϊ̼̼˫�����Ȼ���������ͬ�����ŵķ������G��ͬ���칹�壬���Խ������ű任��Ӧ��λ�õó��䷼�����ͬ���칹�壬��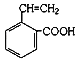 ��
�� ��
��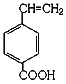 ��
��![]() �����ʴ�Ϊ��
�����ʴ�Ϊ�� ��
�� ��
�� ��
��![]() ������дһ������
������дһ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3.48g������������ȫ�ܽ���100mL 1mol/L�������У�Ȼ�����K2Cr2O7��Һ25 mLǡ��ʹ��Һ�е�Fe2+ȫ��ת��ΪFe3+��Cr2O72-ȫ��ת��ΪCr3+����K2Cr2O7��Һ�����ʵ���Ũ���ǣ� ��
A. 0.05mol/L B. 0.2 mol/L C. 0.1 mol/L D. 0.3 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. 14C��14N��������ͬ����Ϊͬλ�� B. 3He��4He��������ͬ����Ϊͬλ��
C. 12C�� 13N��������ͬ����Ϊͬλ�� D. 12C��14N������ͬ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҳ����ȵ�����������Һϴȥ�Թ��ڱ�մ�е����ʣ�������Ӧ6NaOH��3S![]() 2Na2S��Na2SO3��3H2O�����ڸ÷�Ӧ��˵������ȷ����(����)
2Na2S��Na2SO3��3H2O�����ڸ÷�Ӧ��˵������ȷ����(����)
A. ��������������ǻ�ԭ�� B. �����ǻ�ԭ����
C. ��ȱ����������ֱ��ֻ�ԭ�� D. ����3 mol ��ת�Ƶ���6 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ҵ��Һ�к���Cu2+��Mg2+��Zn2+�����ӣ�Ϊ����������ã����������¹���

��֪Zn��OH��2��������Al��OH��3���ƣ������Լ��������Լ���ѡ��
������ ��п�� ��ϡHNO3 ��ϡH2SO4 ��ϡHCl ��ϡ��ˮ ��NaOH��Һ ��ʯ��ˮ
��ش��������⣺
��1���Լ�1���Լ�2���Լ�3�ֱ������__________________�����ţ�
��2������2������______________ ��________________ �� __________
��3������3��________________________________
��4���ӹ���CO2ʱ������Ӧ�����ӷ���ʽ_________________________________
��5���ڽ���ұ�������з���1��______________����2��_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С���������л�ѧ��Ӧ��ʵ�������Ʊ��������������й��������ʵ��о���MnO2��4HCl(Ũ)![]() MnCl2��Cl2����2H2O
MnCl2��Cl2����2H2O
(1)��С��ͬѧ������ͼ��ʾ�������Լ�(��һ��ȫ��)�Ʊ����ռ������������������


��Ӧ��ѡ���������________(����ĸ)��
��Ũ������������̷�Ӧ�����ӷ���ʽΪ____________________________
(2)��С��ͬѧ��Ʋ��ֱ�������ͼ��ʾװ��̽�������������ԡ�

��G�е�������________��ԭ����__________________(�û�ѧ����ʽ��ʾ)��
��H�������__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Be��OH��2�����Եģ���ǿ�ᷴӦʱ����Be2+����ǿ�Ӧʱ����BeO22�����������ݵ����ʵ���Ũ�ȡ��������BeCl2��MgCl2��AlCl3��Һ������ʱ�������������ᣩ���ֽ�һ��Ũ�ȵ�NaOH��Һ�ֱ����������Һ����������NaOH��Һ�����x��mL�������ɳ��������ʵ���y��mol���Ĺ�ϵ��ͼ��ʾ������BeCl2��MgCl2��AlCl3������Һ��Ӧ��ͼ����ȷ���ǣ�������

A. �ݢۢ� B. �ڢۢ� C. �ۢݢ� D. �ۢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(��)A��B��C��D��E����Ԫ�������ڱ����λ�����±���ʾ��
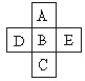
A��B��CΪͬ����Ԫ�أ�AΪ������ԭ�Ӱ뾶��С��Ԫ�أ�D��B��EΪͬ����Ԫ�أ�EΪ��������ԭ�Ӱ뾶��С��Ԫ�ء�DԪ��������____�������ڱ���___���ڣ���______�壬��ԭ�ӽṹʾ��ͼ______��
(��)A��B��C��D��E��F���ֶ�����Ԫ�ص�ԭ����������������֪A��C��F��ԭ�ӵ�����㹲��11�����ӣ���������Ԫ�ص�����������ˮ����֮���������ܷ�Ӧ���������κ�ˮ��DԪ��ԭ�ӵ������������ȴ�����������4����EԪ��ԭ�ӵĴ�����������������������3�����Իش�
(1)д������Ԫ�صķ���A_____��D_____��E_____��
(2)A��C����Ԫ������������ˮ����֮�䷴Ӧ�����ӷ���ʽ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ����ĵ�λ����Ħ���������Ķ����ǣ� ��
A. �̳���Ʒ(���ľߵ�)B. ϸС��Ʒ(��������)
C. ������(����ӵ�)D. ֻ�з��ӡ�ԭ�Ӻ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com