
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
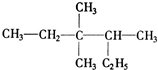 系统命名法命名为
系统命名法命名为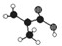 所示(图中球与球之间的连线代表化学键,如单键、双键等).
所示(图中球与球之间的连线代表化学键,如单键、双键等).查看答案和解析>>
科目:高中化学 来源: 题型:
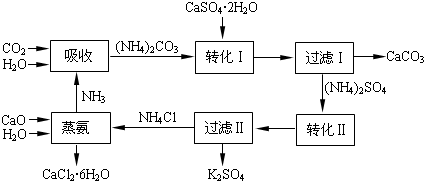
2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
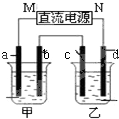 如图装置中甲烧杯盛放100mL 0.2mol?L-1的NaCl溶液,乙烧杯盛放100mL 0.5mol?L-1L的CuCl2溶液.a、b、c、d电极均为石墨,反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞溶液,观察到b电极附近首先变红.
如图装置中甲烧杯盛放100mL 0.2mol?L-1的NaCl溶液,乙烧杯盛放100mL 0.5mol?L-1L的CuCl2溶液.a、b、c、d电极均为石墨,反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞溶液,观察到b电极附近首先变红.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com