
| A. |  | B. | 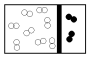 | C. |  | D. |  |
分析 白球代表氢原子,黑球代表氦原子,等质量的氢气与氦气,其物质的量之比=$\frac{mg}{2g/mol}$:$\frac{mg}{4g/mol}$=2:1,相同条件下其体积之比为2:1,据此进行解答.
解答 解:设氢气与氦气都为mg,则二者的物质的量之比为$\frac{mg}{2g/mol}$:$\frac{mg}{4g/mol}$=2:1,则体积之比为2:1;
A.白球代表氢原子,黑球代表氦原子,符合物质的量之比为2:1,体积之比为2:1,故A正确;
B.白球代表氢原子,黑球代表氦原子,物质的量之比=8:2=4:1,且氦气是单原子构成的分子,不满足条件,故B错误;
C.白球代表氢原子,黑球代表氦原子,物质的量之比2:1,但体积之比为1:2,故C错误;
D.白球代表氢原子,黑球代表氦原子,物质的量之比为1:1,体积之比为2:1,故D错误;
故选A.
点评 本题考查阿伏伽德罗定律,题目难度不大,明确等质量的气体中物质的量和体积的关系是解答的关键,并注意氦气的构成来解答.


科目:高中化学 来源: 题型:选择题

| A. | pH=2.7的溶液中:$\frac{{c}^{2}(H{C}_{2}{O}_{4}^{-})}{c({H}_{2}{C}_{2}{O}_{4})×c({C}_{2}{O}_{4}^{2-})}$=10-2.97 | |
| B. | pH=4.27的溶液中,c(K+)+c(H+)=c(OH-)+3c(C2O42-) | |
| C. | 反应HC2O4-+H2O?H2C2O4+OH-的平衡常数为10-4.27 | |
| D. | 向溶液中加KOH溶液将pH由1.30增大至4.27的过程中水的电离程度先增大后减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途.
钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途.查看答案和解析>>
科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O与Na2O2均可与水反应放出氧气 | |
| B. | Na2O和Na2O2中的元素的化合价均相同 | |
| C. | Na2O2与H2O反应为放热反应 | |
| D. | 在呼吸面具中,Na2O常作供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔沸点高低:CH4<SiH4<GeH4<SnH4 | |
| B. | 离子半径大小:Cl-<Mg2+<O2-<F- | |
| C. | 分散质微粒直径大小:Fe(OH)3胶体>CaCO3悬浊液>NaCl溶液 | |
| D. | 酸性强弱:H2SO4<H3PO4<H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 1mol该物质最多消耗2molNaOH | B. | 该物质的分子式为C8H8NO2 | ||
| C. | 该物质能发生取代反应和加成反应 | D. | 该物质苯环上的一溴代物有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铜屑加入 Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+ | |
| B. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O | |
| C. | 将氯化亚铁酸性溶液和H2O2混合:Fe2++2H++H2O2═Fe3++2H2O | |
| D. | 将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| 测定上述实验用的Fe(NO3)3溶液的pH 配制相同pH的稀硝酸 溶液,并将适量此溶液加入有银镜的试管内. | 若银镜消失,假设2成立. 若银镜不消失,假设2不成立. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com