
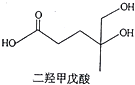
 二羟甲戊酸是生物合成青蒿素的原料之一,下列关于二羟甲戊酸的说法正确的是( )
二羟甲戊酸是生物合成青蒿素的原料之一,下列关于二羟甲戊酸的说法正确的是( )| A. | 与乙醇发生酯化反应生成产物的分子式为C8H18O4 | |
| B. | 能发生加成反应,不能发生取代反应 | |
| C. | 在铜的催化下与氧气反应的产物可以发生银镜反应 | |
| D. | 标准状况下1mol该有机物可以与足量金属钠反应产生22.4L H2 |
分析 由结构可知分子式,分子中含-OH、-COOH,结合醇、羧酸的性质来解答.
解答 解:A.二羟甲戊酸的分子式为C6H12O4,-COOH与乙醇发生酯化反应生成有机产物的分子式为C8H16O4,故A错误;
B.不能发生加成反应,故B错误;
C.含-CH2OH,在铜的催化下与氧气反应的产物为含-CHO,可以发生银镜反应,故C正确;
D.标准状况下1mol该有机物可以与足量金属钠反应产生1.5mol×22.4L/mol=33.6L H2,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意羧酸不能发生加成反应,题目难度不大.


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:选择题
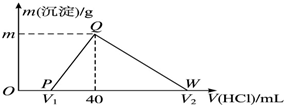 常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol•L-1的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法不正确的是( )
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol•L-1的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法不正确的是( )| A. | OP段发生的反应为:OH-+H+═H2O | B. | 图中V2为100 | ||
| C. | 沉淀的质量m为1.56 g | D. | 原合金质量为0.92 g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;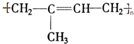 其单体的键线式
其单体的键线式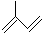 ;
;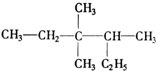 的名称(系统命名法)3,3,4-三甲基已烷.
的名称(系统命名法)3,3,4-三甲基已烷.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 图为浓硫酸与铜片反应的装置.请回答:
图为浓硫酸与铜片反应的装置.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含分子数相等 | B. | 分子间的平均距离相等 | ||
| C. | 分子中的电子总数相等 | D. | 氧原子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2、NaClO中所含化学键类型完全相同 | |
| B. | 只有活泼金属与活泼非金属元素之间才能形成离子键 | |
| C. | D2O和T2O是同一物质 | |
| D. | 氯气与NaOH反应的过程中,同时又离子键、极性键和非极性键的断裂和形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
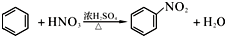
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com