
 ,B的名称是盐酸或硫酸.
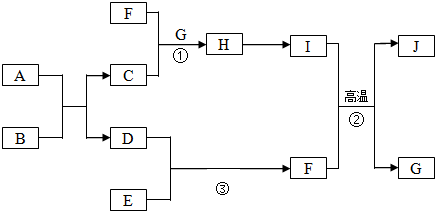
,B的名称是盐酸或硫酸.分析 E是空气中含量最多的单质,则E为N2,A是常见的金属单质,B是常见的强酸,生成的C、D为氯化物和氢气,D能与E反应生成F,则D为H2,所以F为NH3,I是既能与强酸又能与强碱反应的氧化物,则I为Al2O3,G是最常见的无色液体,则G为H2O,J是一种高硬度材料(摩尔质量为41g•mol-1),I和F反应生成G和J,根据元素守恒可知J为AlN,根据物质的转化关系可知H为,C为含铝离子的盐,则A为Al,B可以是盐酸或硫酸,依据推断回答问题.
解答 解:E是空气中含量最多的单质,则E为N2,A是常见的金属单质,B是常见的强酸,生成的C、D为氯化物和氢气,D能与E反应生成F,则D为H2,所以F为NH3,I是既能与强酸又能与强碱反应的氧化物,则I为Al2O3,G是最常见的无色液体,则G为H2O,J是一种高硬度材料(摩尔质量为41g•mol-1),I和F反应生成G和J,根据元素守恒可知J为AlN,根据物质的转化关系可知H为,C为含铝离子的盐,则A为Al,B可以是盐酸或硫酸,
(1)根据上面的分析可知,A为Al,原子核电荷数为13,三个电子层,最外层3个电子,原子结构示意图为: ,B的名称为盐酸或硫酸,
,B的名称为盐酸或硫酸,
故答案为: ,盐酸或硫酸;
,盐酸或硫酸;
(2)反应①的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3•H2O=Al(OH)3↓+3 NH4+;
(3)反应②的化学方程式为:Al2O3+2NH3 $\frac{\underline{\;高温\;}}{\;}$2AlN+3H2O,实验室制备F是氨气是利用氯化铵固体和氢氧化钙固体加热反应生成氯化钙、氨气和水,反应的化学方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑,
故答案为:Al2O3+2NH3 $\frac{\underline{\;高温\;}}{\;}$2AlN+3H2O,2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
点评 本题考查了物质转化关系分析判断,主要是铝及其化合物性质,氮及其化合物性质的分析应用,注意反应特征的理解应用是解题关键,题目难度中等.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:解答题
 某学生在如图所示装置中用苯和液溴制取溴苯,请根据下列实验步骤完成有关问题:
某学生在如图所示装置中用苯和液溴制取溴苯,请根据下列实验步骤完成有关问题: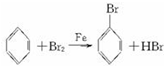 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| B. | 碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ | |
| C. | 往FeCl3溶液中通入H2S气体:2Fe3++H2S═2Fe2++S↓+2H+ | |
| D. | 大苏打溶液中加入稀硫酸:S2O32-+2SO42-+6H+═4 SO2↑+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 焰火中呈现的绚丽色彩,是各种金属元素焰色反应形成的 | |
| B. | 小苏打既是制作糕点的膨松剂,还是治疗胃酸过多的一种药剂 | |
| C. | 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰 | |
| D. | 装运乙醇的包装箱上应贴上易燃液体的危险品标志图标 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Cu和足量浓硝酸反应可收集NO2的分子数为2NA | |
| B. | 4℃时,3.6 mL水所含的电子数为2NA | |
| C. | 30.8g熟石膏(2CaSO4•H2O)中的钙离子数目为0.20NA | |
| D. | 200 mL 0.5mol•L-1的Na2CO3溶液中阴离子数目小于0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com