


科目:高中化学 来源: 题型:
| A、硅元素主要以单质、氧化物、硅酸盐的形式存在于自然界中 |
| B、浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
| C、用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 |
| D、Ca(HCO3)2溶液与过量NaOH溶液反应可制得Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
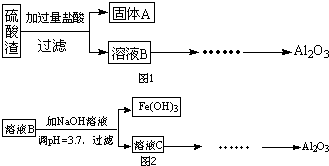 (1)写出溶液B的溶质是
(1)写出溶液B的溶质是查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
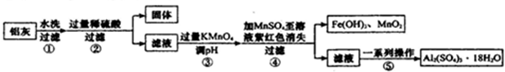
| 物质 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com