


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、葡萄吃起来是酸的,故它属于酸性食物 |
| B、蛋白质在体内经消化后生成碳酸、硫酸、尿酸等,故它属于酸性食物 |
| C、蔬菜、水果多含钾、钠、钙、镁等盐类,习惯称为酸性食物 |
| D、人体具有使血液pH保持正常范围的调控能力,人们可根据自己的口味选择食物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、34g H2O2中含有的阴离子数为NA |
| B、1mol重甲基(-CD3)含有电子数为9NA |
| C、在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
| D、1mol铁铝混合物与足量稀盐酸反应时,转移电子数是3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只含一个双键的直链有机物 |
| B、含两个双键的直链有机物 |
| C、只含一个环的环状有机物 |
| D、只含一个双键的环状有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 和
和 的物质互为同分异构体,我们称之为顺反异构.则分子式为C5H10的有机物,属于烯烃的同分异构体的数目为
的物质互为同分异构体,我们称之为顺反异构.则分子式为C5H10的有机物,属于烯烃的同分异构体的数目为 的二氯代物有
的二氯代物有 的二氯代物有
的二氯代物有查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
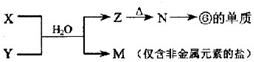
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、位于同一周期的元素原子具有相同的电子层数 |
| B、位于同一主族的元素原子具有相同的最外层电子数 |
| C、IA族元素原子的最外电子层都只有1个电子,所以IA族元素均为活泼金属元素 |
| D、稀有气体元素所在的族称为0族,其原子的最外电子层不都为8电子结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com