
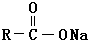 +NaOH$→_{△}^{CaO}$R-H+Na2CO3
+NaOH$→_{△}^{CaO}$R-H+Na2CO3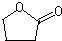 ,K的结构简式为
,K的结构简式为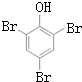 .
.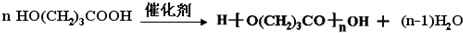 ;
;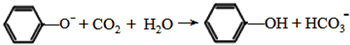 .
.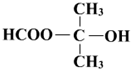 (写结构简式).
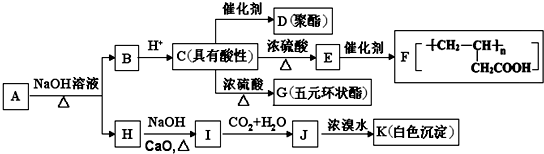
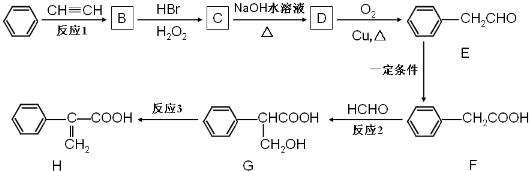
(写结构简式).分析 A在碱性条件下发生水解反应得到B与H,A中含有酯基,B酸化得到C具有酸性,则C中含有羧基,C反应可以得到聚酯,则C中还含有羟基,由F的结构逆推可知E为CH2=CHCH2COOH,C发生消去反应得到E,E发生加聚反应生成F,C在浓硫酸作用下得到五元环状酯G,则C为HOCH2CH2CH2COOH,G为 ,B为HOCH2CH2CH2COONa,C发生缩聚反应得到D为
,B为HOCH2CH2CH2COONa,C发生缩聚反应得到D为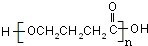 .结合A分子式可知,H中含有7个碳原子,H发生信息中脱羧反应得到H,H与二氧化碳、水作用得到F,F与浓溴水作用是白色沉淀,则F中含有酚羟基,1mol A与足量的NaHCO3反应生成1mol CO2,说明A分子中含有1个-COOH,而A遇FeCl3溶液不显色,则A不含酚羟基,则A中酯基为羧酸与酚形成的,A中含苯环且不含甲基,且苯环上一氯取代物只有2种,则A中含有2个对位位置的取代基,可推知A的结构简式为:
.结合A分子式可知,H中含有7个碳原子,H发生信息中脱羧反应得到H,H与二氧化碳、水作用得到F,F与浓溴水作用是白色沉淀,则F中含有酚羟基,1mol A与足量的NaHCO3反应生成1mol CO2,说明A分子中含有1个-COOH,而A遇FeCl3溶液不显色,则A不含酚羟基,则A中酯基为羧酸与酚形成的,A中含苯环且不含甲基,且苯环上一氯取代物只有2种,则A中含有2个对位位置的取代基,可推知A的结构简式为: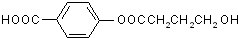 ,H为
,H为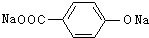 ,I为
,I为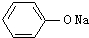 ,J为
,J为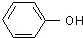 ,K为
,K为 .
.
解答 解:A在碱性条件下发生水解反应得到B与H,A中含有酯基,B酸化得到C具有酸性,则C中含有羧基,C反应可以得到聚酯,则C中还含有羟基,由F的结构逆推可知E为CH2=CHCH2COOH,C发生消去反应得到E,E发生加聚反应生成F,C在浓硫酸作用下得到五元环状酯G,则C为HOCH2CH2CH2COOH,G为 ,B为HOCH2CH2CH2COONa,C发生缩聚反应得到D为
,B为HOCH2CH2CH2COONa,C发生缩聚反应得到D为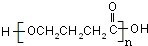 .结合A分子式可知,H中含有7个碳原子,H发生信息中脱羧反应得到H,H与二氧化碳、水作用得到F,F与浓溴水作用是白色沉淀,则F中含有酚羟基,1mol A与足量的NaHCO3反应生成1mol CO2,说明A分子中含有1个-COOH,而A遇FeCl3溶液不显色,则A不含酚羟基,则A中酯基为羧酸与酚形成的,A中含苯环且不含甲基,且苯环上一氯取代物只有2种,则A中含有2个对位位置的取代基,可推知A的结构简式为:
.结合A分子式可知,H中含有7个碳原子,H发生信息中脱羧反应得到H,H与二氧化碳、水作用得到F,F与浓溴水作用是白色沉淀,则F中含有酚羟基,1mol A与足量的NaHCO3反应生成1mol CO2,说明A分子中含有1个-COOH,而A遇FeCl3溶液不显色,则A不含酚羟基,则A中酯基为羧酸与酚形成的,A中含苯环且不含甲基,且苯环上一氯取代物只有2种,则A中含有2个对位位置的取代基,可推知A的结构简式为: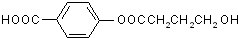 ,H为
,H为 ,I为
,I为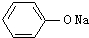 ,J为
,J为 ,K为
,K为 .
.
(1)A为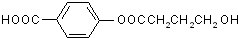 ,有羧基、酯基、羟基3种官能团,H为
,有羧基、酯基、羟基3种官能团,H为 ,分子式为:C7H4O3Na2,
,分子式为:C7H4O3Na2,
故答案为:3;C7H4O3Na2;
(2)由C生成G的反应类型是酯化反应,故答案为:酯化反应;
(3)G的结构简式为 ,K的结构简式为
,K的结构简式为 ,故答案为:
,故答案为: ;
; ;
;
(4)①C→D反应的化学方程式: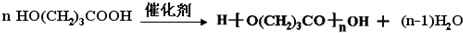 ,
,
②I→J反应的离子方程式: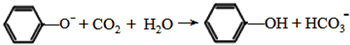 ,
,
故答案为: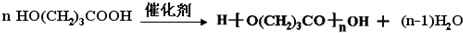 ;
;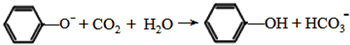 ;
;
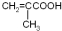
(5)①C为HOCH2CH2CH2COOH,C的同分异构体中能同时满足下列条件:a.能发生银镜反应,说明含有醛基,b.能发生皂化反应,含有甲酸形成的酯基,c.能与Na反应产生H2,还含有羟基,可以看作丙烷中H原子被-OH、-OOCH取代,-OOCH取代甲基中H原子,-OH有3种位置,-OOCH取代亚甲基中H原子,-OH有2种位置,共有5种(不含立体异构),其中核磁共振氢谱显示为3组峰,且峰面积比为6﹕1﹕1的是: ,
,
故答案为:5; ;
;
②C的所有同分异构体中组成元素相同,结构不同,元素分析仪显示的信号(或数据)完全相同,故选:A.
点评 本题考查有机物推断与合成、有机反应类型、同分异构体书写、有机反应方程式等,根据反应条件判断物质含有的官能团,综合分析确定A的结构,侧重考查学生分析推理能力,需要学生熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.06mol.L-1•min-1 | B. | v(H2)=0.04mol.L-1•min-1 | ||
| C. | v(NH3)=0.12mol.L-1•min-1 | D. | v(N2)=0.24mol.L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
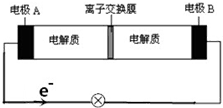 如图装置是一种可充电电池示意图,装置的离子交换膜只允许Na+通过.已知充、放电的化学方程式为2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr,下列说法正确的是( )
如图装置是一种可充电电池示意图,装置的离子交换膜只允许Na+通过.已知充、放电的化学方程式为2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr,下列说法正确的是( )| A. | 充电时,A极应与直流电源正极相连接 | |
| B. | 放电时,当有0.1molNa+通过离子交换膜时,B极上有0.3molNaBr产生 | |
| C. | 放电时,钠离子从左到右通过离子交换膜 | |
| D. | 放电时,负极反应式为3NaBr-2e-═NaBr3+2Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.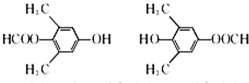 .
. )的合成路线:
)的合成路线: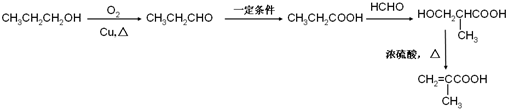 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
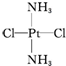 ,黄绿色固体
,黄绿色固体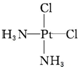 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.8g重水(D2O)中含有的中子数为NA | |
| B. | 1molCl2参加氧化还原反应,转移的电子数一定为2NA | |
| C. | T℃时pH=6的纯水中,含有10-6 NA个OH- | |
| D. | 电解精炼铜时,若转移NA个电子,阴极析出32 g铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
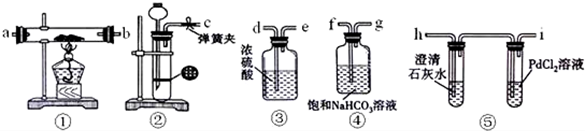
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验序号 | 起始读数/mL | 终点读数/mL |
| I | 2.50 | 22.58 |
| Ⅱ | 1.00 | 23.12 |
| Ⅲ | 0.00 | 19.92 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com