
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:填空题
分某有机物A只含有C、H、O三种元素,16.8g该有机物完全燃烧生成44.0g CO2和14.4g H2O;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O—H键和位于分子端的碳碳三键,核磁共振氢谱有三个峰,峰面积为6﹕1﹕1。
(1)A的分子式是 ;
(2)A的结构简式是 ;
(3)下列物质中,一定条件能与A发生反应的是 (填字母);
A.H2B.Na C.KMnO4 D.Br2
(4)有机物B是A的同分异构体,1mol B可与1mol Br2加成。该有机物所有碳原子在同一个平面,没有顺反异构现象。则B的结构简式是 。B可以用银氨溶液来检验,写出检验的化学方程式
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上月考二化学试卷(解析版) 题型:选择题
恒温恒容,可逆反应:2NO2 2NO+O2
2NO+O2 达到平衡状态的标志是
达到平衡状态的标志是
①单位时间内生成nmolO2的同时生成2nmolNO2
②单位时间内生成nmolO2的同时生成2nmolNO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
A.①④⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省襄阳市四校高一上学期期中化学试卷(解析版) 题型:推断题
A、B、C、D四种可溶性盐,它们的阳离子可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子可能是NO3-、SO42-、Cl-、CO32-的某一种(每种离子只能使用一次);
①若把四种盐分别溶解于盛有蒸馏水的四只试管中,只有C盐的溶液呈蓝色;
②若向四只试管中分别加足量盐酸,B溶液有沉淀产生,D溶液有无色无味气体 逸出。
逸出。
根据①②实验事实可推断它们的化学式为:
(1)A、 ;B、 ;C、 ;D、 ;
(2)写出②中D与盐酸反应的离子方程式: 。
(3)某溶液中含有少量的CaCl2,某学生用过量的D使Ca2+离子转化为沉淀而除去,确认D已过量的实验操作是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省襄阳市四校高一上学期期中化学试卷(解析版) 题型:选择题
下列叙述不正确的是
A.胶体区别于其它分散系的本质特征是:胶体粒子直径在1-100nm之间
B.一定温度、压强下,气体体积由其分子的大小决定
C.氧化还原反应的本质是电子转移
D.在1L2mol/L的氢氧化铁胶体中含有氢氧化铁胶粒数小于2NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省襄阳市四校高一上学期期中化学试卷(解析版) 题型:选择题
PM2.5指大气中直径小于或等于2.5微米(1微米等于10-6m ) 的颗粒物,对空气质量和能见度有重要影响。若将直径为2.5微米颗粒物分散到水中,形成的分散系属于( )
A.溶液 B.胶体 C.浊液 D.不能确定
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期12月月考化学卷(解析版) 题型:选择题
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(己知硝酸只被还原为NO气体)。下列分析或结果错误的是
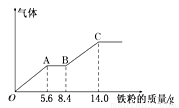
A.H2SO4浓度为2.5mol·L-1
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.原混合酸中NO3-的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上12月考前测试化学卷(解析版) 题型:填空题
一定温度下,有A.盐酸、B.硫酸 、C.醋酸三种酸(用a、b、c回答)。
、C.醋酸三种酸(用a、b、c回答)。
(1)当其物质的量浓度相同时。c(H+)由大到小的顺序是 ,pH由大到小的顺序是 。
(2)同体积、同物质的量浓度的三种酸溶液,中和NaOH的能力由大到小的顺序是 。
(3)当c(H+)相同时 ,物质的量浓度由大到小的顺序为 。
,物质的量浓度由大到小的顺序为 。
(4)当pH相同、体 积相同时,分别加
积相同时,分别加 入足量锌,相同状况下产生的气体体积由大到小的顺序为 。
入足量锌,相同状况下产生的气体体积由大到小的顺序为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一上段考二化学试卷(解析版) 题型:选择题
水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O32-+O2+xOH-=Fe3O4+S4O62-+2H2O,下列说法中错误的是
A.每生成1molFe3O4,反应转移的电子总数为4mol
B.Fe2+和S2O32-都是还原剂
C.1molFe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol
D.x=4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com