
| A、NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O |
| B、铁和稀硝酸反应:Fe+2H+=H2↑+Fe2+ |
| C、向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-=Al(OH)3↓ |
| D、实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,将铁片置于浓硝酸中:Fe+6HNO3=Fe(NO3)3+3NO2↑+3H2O |
| B、向碳酸氢钠溶液中加入少量盐酸:CO32-+2H+═CO2↑+H2O |
| C、向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-=BaSO4↓ |
| D、向浓硝酸中加入铜片:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸丙酯的实验式:CH3COOCH(CH3)2 |
B、聚丙烯的结构简式为: |
C、 的名称:2-甲基丙醇 的名称:2-甲基丙醇 |
D、C2H4的结构式: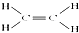 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| H+ |
| H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| H2O/H+ |


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com