
对于反应中的能量变化,表述正确的是()
A. 放热反应中,反应物的总能量大于生成物的总能量
B. 断开化学键的过程会放出能量
C. 加热才能发生的反应一定是吸热反应
D. 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
考点: 化学能与热能的相互转化.
专题: 化学反应中的能量变化.
分析: A、反应物的总能量大于生成物的总能量,该反应放热;
B、旧化学键的断裂需要吸收能量;
C、吸热反应不一定需要加热热才发生,加热才能发生的反应不一定是吸热反应;
D、等质量的硫蒸气具有的能量比硫固体多.
解答: 解:A、大当反应物的总能量大于生成物的总能量时,该反应是放热反应,故A正确;
B、断开化学键的过程会吸收能量,故B错误;
C、吸热反应不一定需要加热热才发生,如氯化铵和十水合氢氧化钡的反应就是吸热的,加热才能发生的反应不一定是吸热反应,如铝热反应,故C错误;
D、等质量的硫蒸气和硫固体相比较,硫蒸气具有的能量多,因此完全燃烧硫蒸气放出的热量多,故D错误.
故选A.
点评: 本题考查学生吸热反应和放热反应的知识,可以根据所学知识进行回答,难度不大.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:
甲、乙两个容器内都进行A→B的反应,甲容器内每分钟减少了4mol A,乙容器内每分钟减少2mol A,则甲容器内的反应速率比乙容器内的反应速率()
A. 快 B. 慢 C. 相等 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
我国成功发射“天宫一号”飞行器的长征Ⅱ火箭推进器中盛有强还原剂肼(N2H4)和强氧化剂液态双氧水(H2O2).当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知此状况下:0.4mol液态肼与足量的液态双氧水反应放出256.0kJ的热量.(已知H2O(l)═H2O(g)△H=+44kJ•mol﹣1)
(1)则16g液态肼与液态双氧水反应在此状况下生成液态水时放出的热量是 kJ.
(2)(2)已知拆开1mol H﹣H键,1mol N﹣H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表示正确的是()
A. 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B. 物质发生化学变化时一定伴随着吸热现象或放热现象
C. 稀溶液中:H+(aq)+OH﹣(aq)=H2O(l);△H=﹣57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含l mol NaOH的溶液混合,放出的热量大于57.3kJ
D. 在25℃101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ的热量,则H2燃 烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=﹣285.8kJ/mol
烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=﹣285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
依据事实,写出下列反应的热化学方程式.
(1)已知拆开1mol H﹣H键,1mol N﹣H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为: .
(2)以甲烷为原料制取氢气是工业上常用的制氢方法.
已知:CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kJ•mol﹣1
CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJ•mol﹣1
请写出CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用化学平衡移动原理解释的是()
A. 合成氨工业中采用高压条件
B. 由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
C. 用排饱和食盐水的方法收集Cl2
D. 反应CO(g)+NO2(g)═CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个容积为VL的密闭容器中放入2LA(g)和1L B(g),在一定条件下发生下列反应:3A(g)+B(g)⇌nC(g)+2D(g),达到平衡后,A物质的量浓度减小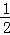 ,混合气体的平均摩尔质量增大
,混合气体的平均摩尔质量增大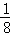 ,则该反应的化学方程式中n的值是()
,则该反应的化学方程式中n的值是()
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
磺化煤(代表式NaR)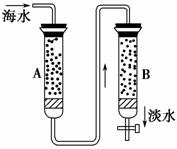 是一种阳离子型交换剂,它能使硬水中的Ca2+、Mg2+通过交换除去而软化。现在海水(已知海水中含Na+、Ca2+、Mg2+等阳离子)的淡化方法是使海水按顺序通过两种离子交换树脂,其流程如右图所示。
是一种阳离子型交换剂,它能使硬水中的Ca2+、Mg2+通过交换除去而软化。现在海水(已知海水中含Na+、Ca2+、Mg2+等阳离子)的淡化方法是使海水按顺序通过两种离子交换树脂,其流程如右图所示。
(1)现有氢型阳离子交换树脂和羟型阴离子交换树脂,则(填代表式)A柱是
________________,B柱是__________________。
(2)按上述顺序装柱的理由是_________________________________________
_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的制备合理的是()
①将氯化铝与硫化钾溶液混合后过滤来制备硫化铝
②将过量的铁与氯气加热反应制备氯化亚铁
③在配制的硫酸亚铁溶液常加入一定量的铁粉和硫酸
④铜先氧化成氧化铜,再与硫酸反应来制取硫酸铜
⑤将45mL水加入到盛有5g氯化钠的烧杯中,溶解配制50g质量分数为5%的氯化钠溶液.
A. 只有④ B. 只有②③ C. 只有③④ D. 全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com