
下列叙述正确的是( )
|
| A. | 在原电池的负极和电解池的阴极上都是发生失电子的氧化反应 |
|
| B. | 用惰性电极电解饱和NaCl溶液,若有1mol电子转移,则生成1mol NaOH |
|
| C. | 用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 |
|
| D. | 镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
考点:
原电池和电解池的工作原理.
专题:
电化学专题.
分析:
A.电解池阴极上得电子发生还原反应;
B.电解饱和氯化钠反应方程式为2NaCl+2H2O 2NaOH+Cl2↑+H2↑,根据氢氧化钠和转移电子之间的关系式计算;
2NaOH+Cl2↑+H2↑,根据氢氧化钠和转移电子之间的关系式计算;
C.用惰性电极电解硫酸钠溶液反应方程式为2H2O O2↑+2H2↑,阴极上生成氢气、阳极上生成氧气;
O2↑+2H2↑,阴极上生成氢气、阳极上生成氧气;
D.作原电池负极的金属加速被腐蚀,作原电池正极的金属被保护.
解答:
解:A.原电池负极上金属失电子发生氧化反应,电解池阴极上得电子发生还原反应,故A错误;
B.电解饱和氯化钠反应方程式为2NaCl+2H2O 2NaOH+Cl2↑+H2↑,若有1mol电子转移,则生成0.5mol氯气生成,所以生成1molNaOH,故B正确;
2NaOH+Cl2↑+H2↑,若有1mol电子转移,则生成0.5mol氯气生成,所以生成1molNaOH,故B正确;
C.用惰性电极电解硫酸钠溶液反应方程式为2H2O O2↑+2H2↑,阴极上生成氢气、阳极上生成氧气,阴阳两极产物的物质的量之比为2:1,故C错误;
O2↑+2H2↑,阴极上生成氢气、阳极上生成氧气,阴阳两极产物的物质的量之比为2:1,故C错误;
D.作原电池负极的金属加速被腐蚀,作原电池正极的金属被保护,在镀锡铁板形成的原电池中铁作负极,加速被腐蚀,镀锌铁板形成的原电池中,锌作负极、铁作正极,铁被保护,所以镀锌铁板更耐腐蚀,故D错误;
故选B.
点评:
本题考查了原电池和电解池原理,明确各个电极上发生的反应是解本题关键,再结合物质之间的关系式计算,题目难度不大.


科目:高中化学 来源: 题型:
把6mol铜粉投入含8mol硝酸和2mol硫酸的稀溶液中,则标准状况下放出的气体的物质的量为( ).
A.2 mol B.3 mol C.4 mol D.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下硝酸铵受热分解的未配平化学方程式为NH4NO3——HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为( )
A.5∶3 B.5∶4
C.1∶1 D.3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:

 H++
H++ 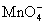 + H2C2O4==== CO2↑+ Mn2++
+ H2C2O4==== CO2↑+ Mn2++
(1)配平以上离子方程式,并在 中填上所需的微粒。
(2)该反应中的还原剂是 。
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为 mol。
(4)测定血钙的含量的方法:取2 mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是 。
②溶解沉淀时 (“能”或“不能”)用稀盐酸,原因是 。
③若消耗了1.0×10-4mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙
g。
查看答案和解析>>
科目:高中化学 来源: 题型:
在2NO2⇌N2O4的可逆反应中,下列状态属于平衡状态的是( )
|
| A. | υ正=υ逆≠0时的状态 | B. | NO2全部转变成N2O4的状态 |
|
| C. | c(NO2)=c(N2O4)的状态 | D. | N2O4不再分解的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
高温下,某反应达平衡,平衡常数K=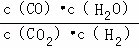 .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
|
| A. | 该反应的焓变为正值 |
|
| B. | 恒温恒容下,增大压强,H2浓度一定减小 |
|
| C. | 升高温度,逆反应速率减小,平衡常数K增大 |
|
| D. | 该反应化学方程式为CO+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在实验室里过滤一种浑浊溶液,发现滤出的液体仍浑浊,他检查实验装置发现漏斗外壁没有水,滤纸也未出现破损或小漏洞,则造成实验失败的原因可能是下列操作中的( )
|
| A. | 滤纸高出漏斗边缘的部分未剪掉 |
|
| B. | 滤纸与漏斗之间有气泡未被排掉 |
|
| C. | 倾倒液体时液面高于滤纸边缘 |
|
| D. | 过滤时玻璃棒靠在一层滤纸一边 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各选项所描述的两个量中,前者一定大于后者的是()
A. pH=3的盐酸的Cl﹣浓度和pH=3的醋酸溶液的CH3COO﹣浓度
B. pH相同的氨水和醋酸钠溶液中,由水电离产生的c(H+)
C. 0.1mol/L的盐酸和0.1mol/L的醋酸分别与金属镁反应的速率
D. pH=11的NaOH和pH=11的氨水分别稀释100倍后的pH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com