
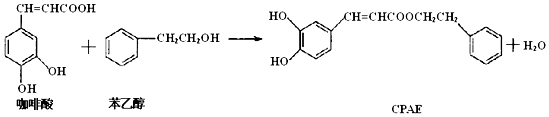
| A. | 咖啡酸分子中所有碳原子可能处在同一个平面上 | |
| B. | 1 mol CPAE与足量的溴水反应,最多消耗3molBr2 | |
| C. | 1 mol 苯乙醇在O2中完全燃烧,需消耗10 mol O2 | |
| D. | 1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH |
分析 A.苯环、乙烯中所有原子共平面,根据乙烯和苯的结构判断咖啡酸中碳原子是否共面;
B.CPAE中苯环上酚羟基的邻对位氢原子能和溴发生取代反应,碳碳双键能和溴发生加成反应;
C.1mol苯乙醇完全燃烧耗氧量=1mol×[n(C)+$\frac{n(H)}{4}$-$\frac{n(O)}{2}$];
D.CPAE中能和NaOH反应的有酯基水解生成的羧基、酚羟基.
解答 解:A.苯环、乙烯中所有原子共平面,根据乙烯和苯的结构知,咖啡酸中所有碳原子可能共平面,故A正确;
B.CPAE中苯环上酚羟基的邻对位氢原子能和溴发生取代反应,碳碳双键能和溴发生加成反应,所有1 mol CPAE与足量的溴水反应,最多消耗4molBr2,故B错误;
C.苯乙醇的分子式为C8H10O,1mol苯乙醇完全燃烧耗氧量=1mol×[n(C)+$\frac{n(H)}{4}$-$\frac{n(O)}{2}$]=1mol×[8+$\frac{10}{4}$-$\frac{1}{2}$]=10mol,故C正确;
D.CPAE中能和NaOH反应的有酯基水解生成的羧基、酚羟基,所有1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH,故D正确;
故选B.
点评 本题考查有机物结构和性质,明确官能团及其性质关系、物质的量的有关计算等知识点是解本题关键,注意酚中苯环上能和溴发生取代反应的位置,知道烃及其衍生物耗氧量的计算方法,题目难度不大.


科目:高中化学 来源: 题型:推断题

 .
.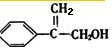 .写出反应⑥的化学方程式(注明必要的反应条件):
.写出反应⑥的化学方程式(注明必要的反应条件): +CH3OH$→_{△}^{浓H_{2}SO_{4}}$
+CH3OH$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O. $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③⑤ | C. | ①③⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 起始加入量(mol) | 平衡时 | ||||
| A | B | C | A或C转化率(%) | C的物质的量分数(%) | 放出或吸收热量(KJ) |
| 1 | 1 | 0 | α1 | φ1 | Q1 |
| 0 | 0 | 2 | α2 | φ2 | Q2 |
| 2 | 2 | 0 | α2 | φ3 | Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验序号号 | 稀硝酸的体积/mL | 剩余固体的质量/g | NO的体积/L |
| 1 | 100 | 17.2 | 2.24 |
| 2 | 200 | 8.00 | 4.48 |
| 3 | 400 | 0 | V |
| A. | 表中 V=7.84 L | |
| B. | 原混合物粉末的质量为25.6 g | |
| C. | 原混合物粉未中铁和铜的物质的量之比为2:3 | |
| D. | 实验3所得溶液中硝酸的物质的量浓度为0.875 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烯的实验式:C3H6 | B. | CO2的电子式: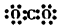 | ||
| C. | 镁离子的结构示意图: | D. | 中子数为18 的氯原子符号:1718Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 131I的质量数为131 | B. | 1mol 131I的质量为131 | ||
| C. | 131I原子核外有5个电子层 | D. | 131I核外最外层电子数为7e- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com