
【题目】在不同温度下按照相同物质的量投料发生反应:CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g) ![]() H<0,测得CO的平衡转化率与压强的关系如图所示,有关说法正确的是 ( )
H<0,测得CO的平衡转化率与压强的关系如图所示,有关说法正确的是 ( )
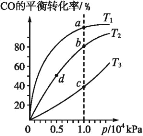
A.反应温度:T1>T2>T3
B.正反应速率:v 正(d)=v 正(b)
C.混合气体密度:ρ(a)>ρ(b)
D.混合气体平均摩尔质量:M(b)<M(c)
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作、现象与结论对应关系正确的是![]()
选项 | 实验操作 | 实验现象 | 结论 |
A | 常温下铜片插入浓硫酸中 | 无明显现象 | 常温下铜被浓硫酸钝化 |
B | 将 | 溶液红色褪去 |
|
C | 等体积 | HX放出的氢气多且反应速率快 | HX酸性比HY弱 |
D | 先向 | 开始有白色沉淀生成;后又有黑色沉淀生成 |
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应热的说法正确的是( )
A.已知甲烷的燃烧热为890.3kJ·mol-1,则表示甲烷燃烧热的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJ·mol-1
B.将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6kJ·mol-1
2NH3(g) ΔH=-38.6kJ·mol-1
C.已知C(石墨,s)=C(金刚石,s) ΔH=+1.9kJ·mol-1,说明金刚石具有的能量比石墨低
D.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.4kJ·mol-1,20g氢氧化钠固体溶于稀盐酸中恰好完全反应时放出的热量大于28.7kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组借助![]() 的仪器装置完成有关实验。
的仪器装置完成有关实验。

(1)用装置A收集NO气体,正确的操作是 ______ ![]() 填序号
填序号![]() 。
。
a.从①口进气,用排水法集气
b.从①口进气,用排气法集气
c.从②口进气,用排水法集气
d.从②口进气,用排气法集气
(2)B装置中的恒压分液漏斗有两个作用,其一是平衡气压使分液漏斗内的液体能顺利滴下,其另一个作用是 ______。
(3)三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通过实验来探究一红色粉末是![]() 、
、![]() 或二者混合物。探究过程如下:
或二者混合物。探究过程如下:
查阅资料:
![]() 是一种碱性氧化物,溶于稀硫酸生成Cu和
是一种碱性氧化物,溶于稀硫酸生成Cu和![]() ,在空气中加热生成CuO
,在空气中加热生成CuO
提出假设:
假设1:红色粉末是![]()
假设2:红色粉末是![]()
假设3:红色粉末是![]() 和
和![]() 的混合物
的混合物
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂。
①若滴加KSCN试剂后溶液不变红色,甲同学认为原固体粉末中一定不含三氧化二铁.乙同学认为其结论不正确,乙同学的理由是 ______。
②若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是 ______。
![]() 经分析,确定红色粉末为
经分析,确定红色粉末为![]() 和
和![]() 的混合物.实验小组欲利用该红色粉末制取较纯净的胆矾
的混合物.实验小组欲利用该红色粉末制取较纯净的胆矾![]() 。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使
。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使![]() 、
、![]() 、
、![]() 分别生成沉淀的pH如下:
分别生成沉淀的pH如下:
物质 |
|
|
|
开始沉淀pH | 6.0 |
|
|
沉淀完全pH | 13 | 14 |
|
实验室有下列试剂可供选择:![]() 氯水
氯水 ![]()
![]()
![]()
实验小组设计如下实验方案:
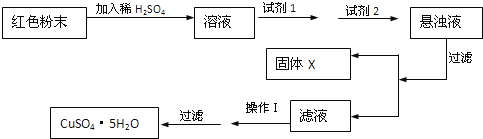
试回答:
①试剂为1____ ![]() 填字母
填字母![]() ,写出溶液中发生反应的离子方程式
,写出溶液中发生反应的离子方程式![]() 写出一个即可
写出一个即可![]() ___。
___。
②试剂为2______ ![]() 填字母
填字母![]() 。
。
③固体X的化学式为 ______。
④操作I为 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学用如下装置电解食盐水,并对电解产物进行探究。
实验装置 | 电解质溶液 | 实验现象 | |
|
| a极附近 | b极附近 |
开始时,产生白色浑浊并逐渐增加,当沉入U形管底部时部分沉淀变为橙黄色;随后a极附近沉淀自下而上也变为橙黄色 | 产生无色气泡 | ||
资料显示:
①氯化亚铜(CuCl)为白色粉末,微溶于水;
②氢氧化亚铜(CuOH)为黄色不溶于水的固体,易脱水分解为红色的![]() ;
;
③![]() 水溶液中不稳定,酸性条件下易歧化为
水溶液中不稳定,酸性条件下易歧化为![]() 和Cu;
和Cu;
④氢氧化铜可以溶于浓NaOH得到蓝色溶液.
![]() 经检验,b极产生的气体是
经检验,b极产生的气体是![]() ,b极附近溶液的pH______
,b极附近溶液的pH______![]() 填“增大”、“减小”、或“不变”
填“增大”、“减小”、或“不变”![]() ;铜丝a应与电源的______
;铜丝a应与电源的______![]() 填“正”或“负”
填“正”或“负”![]() 极相连。
极相连。
![]() 同学们分析a极附近生成的白色浑浊是CuCl,则该极的电极反应式是______。
同学们分析a极附近生成的白色浑浊是CuCl,则该极的电极反应式是______。
![]() ①橙黄色沉淀中含有
①橙黄色沉淀中含有![]() ,则CuCl转化为
,则CuCl转化为![]() 的原因是______
的原因是______![]() 用方程式表示
用方程式表示![]() ;
;
②结合离子在溶液中的运动规律,解释“
![]() 同学们通过实验进一步证实沉淀中含有
同学们通过实验进一步证实沉淀中含有![]() :将橙黄色沉淀滤出洗涤后,滴加
:将橙黄色沉淀滤出洗涤后,滴加![]()
![]() 至过量,应观察到的现象是______。
至过量,应观察到的现象是______。
![]() 同学们根据上述实验提出猜想:电解时,Cu做阳极先被氧化为
同学们根据上述实验提出猜想:电解时,Cu做阳极先被氧化为![]() 。为此,他们用Cu电极电解
。为此,他们用Cu电极电解![]() NaOH溶液,实验时观察到阳极产生大量无色气泡,附近溶液变蓝,未见预期的黄色沉淀。根据现象能否得出“该猜想不成立”的结论,并说明理由:______。
NaOH溶液,实验时观察到阳极产生大量无色气泡,附近溶液变蓝,未见预期的黄色沉淀。根据现象能否得出“该猜想不成立”的结论,并说明理由:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某气态化石燃料X中只含有碳、氢两种元素,为探究该气体中碳和氢两种元素的质量比,某同学设计了燃烧法测量的实验方案,通过测量装置C和D的增重即可求得碳和氢两种元素的质量比.实验装置如下图所示![]() 已知CuO可以作为碳氢化合物燃烧的催化剂
已知CuO可以作为碳氢化合物燃烧的催化剂![]() :
:

(1)若A装置中所盛放的药品是浓NaOH溶液,装置A的作用有:
①______;
②______
(2)D装置中所盛放的药品是______,
(3)E装置的作用是______,
(4)上述装置中有一处缺陷,请改正______.
(5)若实验装置经过改正后,得到的实验数据如下:
质量 | 实验前 | 实验后 |
药品 |
|
|
药品 |
|
|
则该气体中碳和氢两种元素的质量比为______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验课题小组的同学在实验室利用新制备的硫酸亚铁溶液制备硫酸亚铁铵![]() 俗名为莫尔盐
俗名为莫尔盐![]() (
(![]() )
)![]() 相对分子质量为
相对分子质量为![]() ,该晶体比一般亚铁盐稳定,易溶于水,不溶于乙醇。
,该晶体比一般亚铁盐稳定,易溶于水,不溶于乙醇。
(一)制备硫酸亚铁溶液![]() 实验步骤如下
实验步骤如下![]()
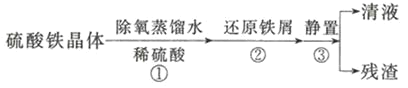
(1)步骤①,加入稀硫酸的目的是________。
(2)步骤②,加入还原铁屑后观察到的现象是________。
实验前,常用碱溶液洗涤铁屑,其目的是________。
(二)制备莫尔盐![]() 硫酸亚铁铵
硫酸亚铁铵![]()
(3)在![]() 溶液中加入稍过量的硫酸铵饱和溶液。从溶液中提取
溶液中加入稍过量的硫酸铵饱和溶液。从溶液中提取![]() 的具体操作是________、用乙醇洗涤、干燥。
的具体操作是________、用乙醇洗涤、干燥。
(三)检验莫尔盐加热时的分解产物
莫尔盐受热分解,甲同学认为分解产物可能有以下几种情况:
![]() 、
、![]() 、
、![]() 、
、![]()
![]() 、
、![]() 、
、![]() 、
、![]()
![]() 、
、![]() 、
、![]() 、
、![]()
![]() 、
、![]() ,
,![]() 、
、![]() 、
、![]()
(4)经认真分析,推理即可确定猜想________![]() 填序号
填序号![]() 不成立。
不成立。
(5)乙同学认为莫尔盐分解的产物中可能含有![]() 、
、![]() 及
及![]() 。为验证产物的存在,乙同学用下列装置进行实验:
。为验证产物的存在,乙同学用下列装置进行实验:
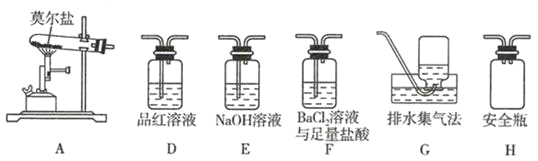
①乙同学的实验中,装置依次连接的合理顺序为![]() ________
________![]() 。
。
②证明分解产物中含有![]() 的实验现象是________。
的实验现象是________。
(四)测定实验![]() 二
二![]() 所得晶体中
所得晶体中![]() 的纯度称取
的纯度称取![]() 硫酸亚铁铵样品配制成
硫酸亚铁铵样品配制成![]() 溶液,取
溶液,取![]() 样品溶液进行实验,装置如图所示。
样品溶液进行实验,装置如图所示。
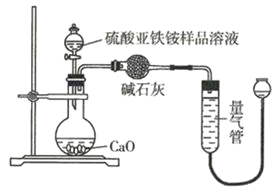
(6)若实验测得![]() 的体积为
的体积为![]() 已折算为标准状况下
已折算为标准状况下![]() ,则该硫酸亚铁铵样品的纯度为________
,则该硫酸亚铁铵样品的纯度为________![]() 列出计算式即可
列出计算式即可![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚氯乙烯是制作装修材料的最常用原料,失火时聚氯乙烯在不同的温度下,发生一系列复杂的化学变化,产生大量有害气体,其过程大体如图所示:

下列说法不正确的是( )
A.上述反应中①属于消去反应,④属于(脱氢)氧化反应
B.聚氯乙烯的单体可由乙烯与HCl加成而得
C.火灾中由聚氯乙烯产生的有害气体中含HCl、CO、C6H6等
D.在火灾现场,可以用湿毛巾捂住口鼻,并尽快远离现场
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面两表分别列出了CO和![]() 的某些性质及相关键能,有关说法不正确的是
的某些性质及相关键能,有关说法不正确的是
表1:
分子 | 熔点 | 沸点 | 常温时在水 中溶解度 |
CO |
|
|
|
|
|
|
|
表2:
CO |
|
|
|
键能 |
|
| |
|
|
|
|
键能 | 193 | 418 | 946 |
A.CO与![]() 的价电子总数相等
的价电子总数相等
B.由表2可知,CO的活泼性不及![]()
C.由表1可知,CO的熔沸点高于![]() ,是因为CO分子间作用力大于
,是因为CO分子间作用力大于![]()
D.由表1可知,室温时,CO在水中的溶解性大于![]() ,是因为CO分子有弱极性
,是因为CO分子有弱极性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com