
【题目】据《科技日报》报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以H2O2为氧化剂直接将CH4氧化成C的含氧化合物。请回答下列问题:
(1)在Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”(指能量相同的原子轨道在全满、半满、全空状态时,体系的能量最低),该原子的外围电子排布式为__。
(2)在第四周期所有元素中,基态原子未成对电子数最多的元素是__(填元素符号)。
(3)金属晶体热导率随温度升高会降低,其原因是__。
(4)铜的焰色反应呈___。在现代化学中,常用于区分晶体与非晶体的方法为___。
(5)Mn和Co的熔点较高的是___,原因___。
(6)钴晶胞和白铜(铜镍合金)晶胞分别如图1、2所示。
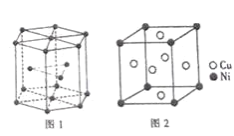
①钴晶胞堆积方式的名称为__;
②已知白铜晶胞的密度为dg·cm-3,NA代表阿伏加德罗常数的值。图2晶胞中两个面心上铜原子最短核间距为__pm(列出计算式)。
【答案】3d104s1 Cr 电子气中的自由电子在热的作用下与金属原子频繁碰撞(温度升高电阻增大) 绿 X-射线衍射法 Co 价电子数多半径小金属键强 六方最密堆积 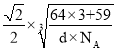 ×1010
×1010
【解析】
(1)在Fe、Co、Ni、Cu中,Cu遵循“洪特规则特例”,3d轨道为全满状态;
(2)在第四周期所有元素中,基态原子最多有6个未成对电子;
(3)金属通过自由电子与金属离子碰撞导热;
(4)x射线衍射法是一种研究晶体结构的方法;
(5)金属键越强,金属晶体的熔点越高;
(6)先根据晶体的密度计算晶胞的边长,再计算两个面心上铜原子最短核间距;
(1)在Fe、Co、Ni、Cu中,Cu遵循“洪特规则特例”,3d轨道为全满状态,Cu原子的外围电子排布式为3d104s1;
(2)在第四周期所有元素中,基态原子未成对电子数最多的原子,外围电子排布式为3d54s1,该元素符号是Cr;
(3)电子气中的自由电子在热的作用下与金属原子碰撞的概率增大,这样电子气不易将动能传远,导热率自然下降;
(4)铜的焰色反应呈绿色。在现代化学中,对固体进行X射线衍射实验区分晶体与非晶体, 所以区分晶体与非晶体的方法为X-射线衍射法;
(5)Mn和Co相比,Co价电子数多、半径小, Co金属键强,所以熔点较高的是Co;
(6)①图1为六方晶胞,所以钴晶胞堆积方式是六方最密堆积;
②设晶胞的边长为a pm,则晶胞的体积为![]() ,根据均摊原则,1个晶胞含有铜原子数是
,根据均摊原则,1个晶胞含有铜原子数是![]() 、镍原子数是
、镍原子数是![]() ,
,![]() ,
,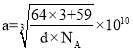 ,晶胞中两个面心上铜原子最短核间距为
,晶胞中两个面心上铜原子最短核间距为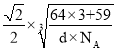 ×1010。
×1010。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.增大压强使平衡向生成Z的方向移动
C.在25℃下,反应的平衡常数为1600,改变温度可以改变此反应的平衡常数
D.在25℃下,测得c(X)=0.04mol·L-1,c(Y)=0.1mol·L-1,c(Z)=0.08mol·L-1,则此时v正<v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对达到平衡状态的可逆反应X+Y![]() Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则下列说法正确的是
Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则下列说法正确的是
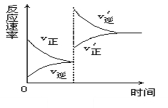
A.X、Y均为气体,Z、W中有一种为气体
B.Z、W中至少一种是气体,X、Y皆非气体
C.X、Y、Z、W皆非气体
D.Z、W均为气体,X、Y中有一种是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单萜类化合物香叶醇是香精油的主要成分之一。在酸性溶液中,香叶醇可以转化为环状单萜α—松油醇:

![]()
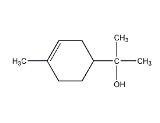
关于香叶醇和α—松油醇,下列说法正确的是( )
A.香叶醇能在铜丝催化下和氧气氧化生成醛,但α—松油醇不能
B.两者互为同分异构体,分子式是C10H20O
C.两者分子中所有原子均处于同一平面
D.两者均能使溴的四氯化碳溶液褪色,是发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同容积的4个密闭器中进行同一种可逆反应,2A(g)+B(g)![]() 3C(g)+2D(g),起始时4个容器所盛A、B的量如表所示各容器所盛物质的量:
3C(g)+2D(g),起始时4个容器所盛A、B的量如表所示各容器所盛物质的量:
容器 | 甲 | 乙 | 丙 | 丁 |
A | 2mol | 1mol | 2mol | 1mol |
B | 1mol | 1mol | 2mol | 2mol |
在相同温度下,建立平衡时,4个容器中A或B的转化率的大小关系是
A.A的转化率为:甲<丙<乙<丁B.A的转化率为:甲<乙<丙<丁
C.B的转化率为:甲>丙>乙>丁D.B的转化率为:丁>乙>丙>甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向 100 mL 蒸馏水中滴入10 mL 5 mol·L-1HA溶液,利用传感器测得溶液中 c (H+)和温度随着加入 HA 溶液体积的变化曲线如图所示,下列有关说法正确的是

A.HA 是强酸
B.a ~ b 段,HA 电离放热,使溶液温度升高
C.c ~ d 段, c (H+)增大,HA 电离程度增大
D.c 点时,加入等体积等浓度的 NaOH 溶液,则 c (Na+)= c (A-)+ c (HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度和压强下,将等质量的CH4、CO2、O2、SO2四种气体分别吹入四个不同的气球,下列说法中正确的是( )

A.气球②中装的是O2
B.气球①和气球③中气体分子数相等
C.气球①和气球④中气体物质的量之比为4∶1
D.气球③和气球④中气体密度之比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在20mL0.1molL﹣1NaOH溶液中逐滴加入0.2molL﹣1的某一元弱酸HX溶液,曲线如图所示,有关粒子浓度关系的比较中,错误的是( )
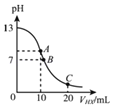
A.在A点:c(Na+)>c(OH﹣)>c(X﹣)>c(H+)
B.在B点:c(OH﹣)=c(H+)=c(Na+)=c(X﹣)
C.在C点:c(X﹣)>c(Na+)>c(H+)>c(OH﹣)
D.在C点:c(X﹣)+c(HX)=2c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com