
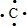 ,B为O元素,形成的两种同素异形体的化学式为O2、O3,C为Na元素,其离子结构示意图为:
,B为O元素,形成的两种同素异形体的化学式为O2、O3,C为Na元素,其离子结构示意图为: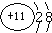 ,
,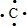 ;O2、O3;
;O2、O3;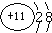 ;
;
| ||
| ||


科目:高中化学 来源: 题型:
| A、回收废旧电池 |
| B、使用无磷洗衣粉 |
| C、开发燃料电池汽车,消除机动车尾气污染 |
| D、加高工厂的烟囱,使烟尘和废气远离地表 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、白磷在260℃转化成红磷 |
| B、石墨在高温高压下转化为金刚石 |
| C、干冰转变为CO2气体 |
| D、固态S8加热到444.6℃时变成硫蒸气S2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
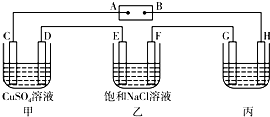 如图所示的装置,C、D、E、F均为惰性电极.将电源接通后,向乙中滴入酚酞溶液,在F极附近显红色.试回答下列问题:(1)电极A是
如图所示的装置,C、D、E、F均为惰性电极.将电源接通后,向乙中滴入酚酞溶液,在F极附近显红色.试回答下列问题:(1)电极A是查看答案和解析>>
科目:高中化学 来源: 题型:
| H | + 4 |
c
| ||
| c(NH3?H2O) |
| c(NH3?H2O) |
| c(OH-) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com