
| �� | �� | �� | �� | �� | �� | |
| ��������ɷ� | Fe��Cu | Cu | Cu | - | - | - |
| ��Һ�еĽ������� |
| �� | �� | �� | �� | �� | �� | |
| ��Һ�еĽ������� | Fe2+ | Fe2+ | Fe2+��Cu2+ | Fe2+��Cu2+ | Fe2+��Fe3+��Cu2+ | Cu2+��Fe3+ |
| 8(1-x) |
| 3 |
| 8x |
| 3 |
| 8(1-x) |
| 3 |
| 8x |
| 3 |
| 8 |
| 3 |
| 8x |
| 3 |
| 8x |
| 3 |
| x |
| 3 |
| 8 |
| 3 |
| x |
| 3 |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� | �� | �� | �� | �� | �� | |
| ��������ɷ� | Fe��Cu | Cu | Cu | - | - | - |
| ��Һ�еĽ������� |
| 8 |
| 3 |
| x |
| 3 |
| 8 |
| 3 |
| x |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)�����ӷ�����д���пհ�(�оٳ�ȫ�����ܵ����)
| �� | �� | �� | �� | �� |
��������ɷ� |
|
|
|
|
|
��Һ�еĽ������� |
|
|
|
|
|
(2)����Һ�н�������ֻ��Fe2+��Cu2+ʱ����b��ȡֵ��Χ��__________________(��a��x��ʾ)��
(3)��x=0.5����Һ��Fe3+��Fe2+�����ʵ������ʱ���ڱ�״���¹�����672 mL���塣��a��b��ֵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(1)��HNO3���������ӣ���Һ�еĽ������ӺͲ�������ijɷ�����������������������ӷ�����д���пհף�
| �� | �� | �� | �� | �� | �� |
��Һ�еĽ������� |
| Fe2+ |
| Fe2+ Cu2+ |
| Cu2+ Fe3+ |
��������ɷ� | Fe Cu |
| Cu | �� | �� | �� |
(2)����Һ�н�������ֻ��Fe2+��Cu2+ʱ����b��ȡֵ��Χ��?
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���Ϻ����ֶ������߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
����Fe��Cu��ɵĺϽ�����Cu��Fe�������ʵ���Ϊa mol��Cu�����ʵ�������Ϊx���гɷ�ĩ��ȫ��Ͷ�뺬b mol HNO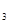 ��ϡ��Һ�У���ʹ���ַ�Ӧ��������Ļ�ԭ����ֻ��NO���Իش��������⣺
��ϡ��Һ�У���ʹ���ַ�Ӧ��������Ļ�ԭ����ֻ��NO���Իش��������⣺
��1����ʣ��IJ���ֻ��Cu������Һ�к��еĽ�������Ϊ__________��(д�����п������)
��2������Һ�н�������ֻ��Fe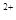 ��Cu
��Cu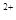 ʱ����b��ȡֵ��Χ��(��a��x��ʾ)___________��
ʱ����b��ȡֵ��Χ��(��a��x��ʾ)___________��
��3����x��0.5����Һ��Fe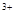 ��Fe
��Fe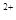 �����ʵ������ʱ���ڱ�״���¹�����672 mL���塣��a��____________��b��_____________��
�����ʵ������ʱ���ڱ�״���¹�����672 mL���塣��a��____________��b��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Fe��Cu��ɵĺϽ�����Cu��Fe�������ʵ���Ϊamol��Cu�����ʵ�������Ϊx���гɷ�ĩ��ȫ��Ͷ�뺬bmol HNO3��ϡ��Һ�У���ʹ���ַ�Ӧ��������Ļ�ԭ����ֻ��NO���Իش��������⣺(��֪��Cu+2Fe3+=2Fe2++Cu2+)
��1����HNO3���������ӣ���Һ�еĽ������ӺͲ�������ijɷ�����������������������ӷ�����д���пհף�
| �� | �� | �� | �� | �� | �� |
��Һ�еĽ������� |
| Fe2+ |
| Fe2+��Cu2+ |
| Cu2+��Fe3+ |
��������ɷ� | Fe��Cu |
| Cu | �D�D | �D�D | �D�D |
��2������Һ�н�������ֻ��Fe2+��Cu2+ʱ����b��ȡֵ��Χ��
��3����x=0.5ʱ����Һ��Fe3+��Fe2+�����ʵ������ʱ���ڱ�״��������672mL���塣��a��b��ֵ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com