
| A.试样中含有加热易挥发的杂质 | B.加热后不是在于燥器中冷却试样 |
| C.实验前坩埚来完全干燥 | D.加热时有晶体溅出 |
科目:高中化学 来源:不详 题型:实验题
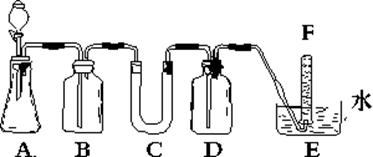
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
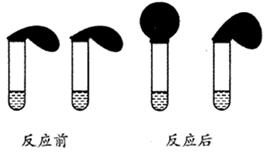
| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后最高 或最低温度 |
| ① | 35mL水 | 2.5g NaHCO3固体 | 20℃ | 18.5℃ |
| ② | 35mL水 | 3.2 Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 35mL稀盐酸 | 含2.5g NaHCO3的饱和溶液32.5mL | 20℃ | 19℃ |
| ④ | 35mL稀盐酸 | 含3.2g Na2CO3的饱和溶液23.1mL+10ml水 | 20℃ | 24.2℃ |
| ⑤ | 35mL稀盐酸 | 2.5gNaHCO3固体 | 20℃ | 16.2℃ |
| ⑥ | 35mL稀盐酸 | 3.2g Na2CO3固体 | 20℃ | 25.1℃ |
| A.NaHCO3的溶解是吸热过程 |
| B.NaHCO3的饱和溶液和盐酸的反应是吸热反应 |
| C.Na2CO3的溶解是放热过程 |
| D.Na2CO3的饱和溶液和盐酸的反应是吸热反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
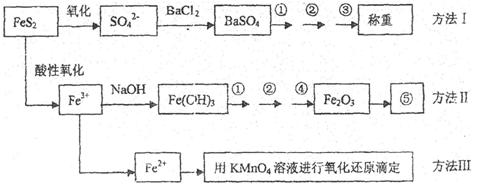
| A.砝码生锈 | B.定容时俯视 |
| C.称量时物质和砝码位置反了(需要游码) | D.容量瓶用待装液润 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在托盘天平的两托盘中分别放等质量的纸,称取2.0g NaOH固体 |
| B.将NaOH固体在烧杯中溶解后迅速小心转移至250mL容量瓶中 |
| C.定容时不小心加水超过了刻度线,此时迅速用胶头滴管吸出一些 |
| D.溶液配置完毕,立即将其转移至带橡胶塞的试剂瓶,贴上标签并洗涤容量瓶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用浓氢氧化钠溶液除去氯气中少量的氯化氢 |
| B.加入稀硝酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-存在 |
| C.食盐中的碘可以直接用淀粉检验其是否存在 |
| D.用干燥的pH试纸可测得新制氯水的pH=2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
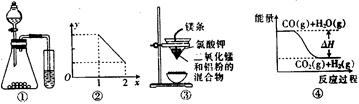
| A.用图①实验装置可完成比较乙酸、碳酸、苯酚三者酸性强弱的实验 |
| B.图②表示NOx溶于水完全转化为HNO3时,x与耗氧量y之间的关系 |
| C.用图③装置可制得金属锰 |
D.图④表示可逆反应CO2 (g)+H2(g) CO(g)+H2O(g)的△H<O CO(g)+H2O(g)的△H<O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.试样 产生银镜结论:该试样是醛类 产生银镜结论:该试样是醛类 |
B. 某卤代烃试样 某卤代烃试样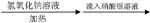 最终的沉淀不是白色; 最终的沉淀不是白色;结论:该卤代烃中不含氯原子 |
C.某 溶液 溶液 冒着白雾 冒着白雾 产生大量白烟; 产生大量白烟;结论:此溶液为浓盐酸 |
D.无色试液 呈黄色;结论:此溶液一定含有钠元素 呈黄色;结论:此溶液一定含有钠元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.配制0.1mol/L的盐酸500mL,应选用的仪器有胶头滴管、烧杯、玻璃棒、天平、500mL容量瓶 |
| B.欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
| C.为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量 |
| D.测定硫酸铜晶体中结晶水含量, 加热坩埚中晶体完全失水后需在空气中冷却,再称量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com