
����˵����ȷ����
A��Ϊȷ��ij��H2A��ǿ�ỹ�����ᣬ�ɲ�NaHA��Һ��pH����pH��7����H2A�������pH��7����H2Aһ����ǿ��
B������֪Ũ�ȵ�����ζ�δ֪Ũ�ȵİ�ˮ��ѡ�����ָʾ��Ϊ��̪
C������50ml 0.55mol/L��NaOH��Һ���ֱ���50ml 0.50mol/L�������50ml 0.50mol/L�������ַ�Ӧ������Ӧ���к������
D����ͬ�¶��£��������Ȼ�������ֱ������ͬ����Ģ�����ˮ����0.1 mol/L���ᡢ��0.1 mol/L�Ȼ�þ��Һ����0.1 mol/L��������Һ�У�Ag��Ũ�ȣ��٣��ܣ��ڣ���
C
��������
���������A. ��NaHA��Һ��pH����pH>7��˵��HA�D ��ˮ����ڵ���, ��H2A�����H2A�����ᣬpHҲС��7��A����B.��ˮ�����������ȫ���룬ǡ�÷�Ӧ������ǿ�������Σ���Һ�����ԣ�ѡ������ã�B����C. ǿ���ǿ����кͷ�Ӧ����1 molҺ̬ˮʱ���ͷŵ����������к��ȣ��к����Ƕ�ֵ��C��ȷ��D����ȷ�������Ȼ��������ڢ�����ˮ���������0��1 mol/L�����е���̶ȼ�С ��0��1 mol/L�Ȼ�þ��Һ��Cl�D Ϊ0��2 mol/L��AgCl����С�ڢ��еĵ��룻��0��1 mol/L��������Һ��Ag�� Ũ���������Ag+Ũ�ȣ���>��>��>��,D����ѡC��
���㣺����������ʵĵ���ƽ�⼰��Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����Ļ�������������һ�и�һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������������ɢϵ��ʵ����
A������ɷ��������ЧӦ
B�����������ܹ����������˶�
C������������ֽ����������ֽ
D����������ֱ����1nm��100nm֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭�ո����и�һ��ѧ�����е��в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ��ʵ�鷽��Ϊ����̽�����������ṩ��һ�ѽ�Կ�ס�����ʵ�鷽����ȷ����
A��ʵ���ҿ�ͨ������ķ������Ӻ�Fe3��������ˮ�л����������ˮ
B������Ʒ�м��������ữ���Ȼ�����Һ����ȷ����Ʒ���Ƿ���SO42?
C���ýྻ�IJ�����պȡ����Һ��Ʒ��Һ���ھƾ��ƻ��������գ�����Ƿ���Na+
D���ø����ҽྻ�IJ�����պȡ������Һ����ʪ���pH��ֽ�в���������ɫ�����տɲⶨ��Һ��pHֵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭�ո����и�һ��ѧ�����е��в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
С������ѪҺ���鵥�У�������Ϊ5.9��10��3 mol��L��1 ����ʾ�����ָ�����������
A���ܽ��(s) B�����ʵ���Ũ��(c)
C����������(w) D��Ħ������(M)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�¶��£���һ�����0.1mol/L�Ĵ�����Һ����μ���0.1mol/L��NaOH��Һ����Һ��pOH(pOH=-lg[OH-])��pH�ı仯��ϵ��ͼ��ʾ����
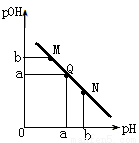
A��M����ʾ��Һ��������ǿ��Q��
B��N����ʾ��Һ��C(CH3COO-)>C(Na+)
C��M���N����ʾ��Һ��ˮ�ĵ���̶���ͬ
D��Q������NaOH��Һ��������ڴ�����Һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�pH=13��ǿ����Һ��pH=2��ǿ����Һ��ϣ�������Һ��pH=11����ǿ����ǿ��������
A��11��1 B��9��1 C��1��11 D��1��9
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��CH3OH(g)+H20(g)=CO2(g)+3H2(g) ��H=+49��O kJ��mol
��CH3OH(g)+1/202(g)=CO2(g)+2H2(g) ��H=-192��9 kJ��mo1

����˵����ȷ����
A��CH30Hת���H2�Ĺ���һ��Ҫ��������
B���ٷ�Ӧ�У���Ӧ��������������������������
C�����ݢ���֪��Ӧ��CH3OH(l)+1/202(g)=CO2(g)+2H2(g) ��H>һ192��9 kJ��mol
D����Ӧ�ڵ������仯��ͼ��ʾ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��һ��ѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ʯ��ˮ��С�մ��ۺ�ʳ�Ȳ�����ɵ�ʵ���ǣ�
A����������Ҫ�ɷֵļ��� B��ʳ�κʹ���ļ���
C�������е�ļ��� D��ůƿ��ˮ���ij�ȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��㶫ʡ��ɽ�и߶���ѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ��������ȷ��ʾ��Ӧ������ǣ�
A����ϩ�Ľṹ��ʽC2H4 B������Ľṹ��ʽCH3��CH2��2CH3
C�����Ȼ�̼�Ľṹʽ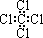 D�����ķ���ʽ
D�����ķ���ʽ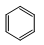
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com