
【题目】X、Y、Z、M是原子序数依次增大的短周期主族元素,Y的最外层电子数是内层电子数的3倍,Y与Z形成的化合物Z2Y3中,元素质量比m(Y):m(Z)=8:9;X原子的最外层电子数为M原子和Z原子最外层电子数的和的一半。下列说法正确的是
A.X的最高价氧化物对应的水化物一定为强酸B.气态氢化物的沸点:Y>M
C.Z是地壳中含量最多的元素D.原子半径:Z>M>X>Y
【答案】BD
【解析】
X、Y、Z、M是原子序数依次增大的短周期主族元素,Y的最外层电子数是内层电子数的3倍,则Y为氧元素;Y与Z 形成的化合物Z2Y3中,元素质量比m(Y):m(Z)=8:9,则Z的相对原子质量为![]() ,故Z为铝元素;X原子的最外层电子数为M原子和Z原子最外层电子数的和的一半,而M原子序数大于Z,故X最外层电子数大于3小于6,若为4,则X为碳元素,M为磷元素;若为5,则X为氮元素,M为氯元素。
,故Z为铝元素;X原子的最外层电子数为M原子和Z原子最外层电子数的和的一半,而M原子序数大于Z,故X最外层电子数大于3小于6,若为4,则X为碳元素,M为磷元素;若为5,则X为氮元素,M为氯元素。
A. 若X为碳元素,则其最高价氧化物的水化物碳酸是弱酸,A错误;
B. 无论M是磷元素还是氯元素,因H2O存在氢键,气态氢化物的沸点:Y>M,B正确;
C. 地壳中含量最多的元素是O,C错误;
D. 同一周期从左往右,原子半径越来越小,同一主族从上往下,原子半径越来越大,所以无论M是磷元素还是氯元素,原子半径Z>M>X>Y,D正确。
答案选BD。


科目:高中化学 来源: 题型:
【题目】关于下列各实验装置的叙述中,不正确的是( )
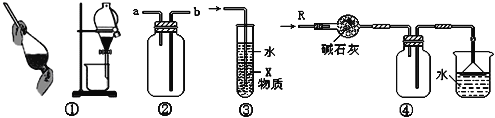
A. 装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
B. 装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
C. 装置①可用于分离C2H5OH和H2O的混合物
D. 装置④可用于干燥、收集NH3,并吸收多余的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为![]() 时,在三个容积均为
时,在三个容积均为![]() 的恒容密闭容器中仅发生反应:
的恒容密闭容器中仅发生反应:![]() 正反应吸热
正反应吸热![]() 。实验测得:
。实验测得:![]() ,
,![]() ,
,![]() 、
、![]() 为速率常数,受温度影响。平衡常数
为速率常数,受温度影响。平衡常数![]() 是用平衡分压代替平衡浓度计算,分压
是用平衡分压代替平衡浓度计算,分压![]() 总压
总压![]() 物质的量分数。下列说法不正确的是
物质的量分数。下列说法不正确的是![]()
![]()
容器 编号 | 物质的起始浓度 | 物质的平衡浓度 | ||
|
|
|
| |
Ⅰ |
| 0 | 0 |
|
Ⅱ |
|
|
| |
Ⅲ | 0 |
|
| |
A.达平衡时,容器Ⅱ中![]() 比容器Ⅰ中的小
比容器Ⅰ中的小
B.容器Ⅱ反应达平衡前,![]()
C.起始时容器Ⅰ中总压强为![]() ,则
,则![]() 时该反应的平衡常数
时该反应的平衡常数![]() kPa
kPa
D.当温度改变为![]() 时,若
时,若![]() 则
则![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用硫铁矿烧渣(主要成分为![]() 、
、![]() 、FeO、
、FeO、![]() 等)为原料来制取氧化铁。
等)为原料来制取氧化铁。

请回答下列问题
(1)酸溶过程中发生反应的离子方程式是:______;
(2)为了提高酸浸时的速率,除了适当增大硫酸的浓度外,还可以采取的措施有:______![]() 写出两条
写出两条![]() ;
;
(3)检验步骤Ⅲ反应后的溶液中金属阳离子的试剂是:______;
(4)步骤Ⅴ中,![]() 达到沉淀溶解平衡时,室温下测得溶液的pH为8,c(Fe2+)为1.0×10-5mol/L,是判断所得
达到沉淀溶解平衡时,室温下测得溶液的pH为8,c(Fe2+)为1.0×10-5mol/L,是判断所得![]() 中是否混有
中是否混有![]() ______
______![]() 填是或否
填是或否![]() ,请通过简单计算说明理由(已知Ksp[Fe(OH)2]= 4.9×10-17)______;
,请通过简单计算说明理由(已知Ksp[Fe(OH)2]= 4.9×10-17)______;
(5)步骤Ⅴ反应成![]() 的离子反应方程式:______;
的离子反应方程式:______;
(6)欲测定硫铁矿烧渣中Fe元素的质量分数,称取wg样品,充分酸溶、水溶后过滤,向滤液中加入足量的![]() ,充分反应后加入NaOH溶液至不再产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称的残留固体为ng。该样品中Fe元素的质量分数为______
,充分反应后加入NaOH溶液至不再产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称的残留固体为ng。该样品中Fe元素的质量分数为______![]() 用w、n的代数式表示
用w、n的代数式表示![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下合成乙烯:![]() 。已知温度对
。已知温度对![]() 的平衡转化率和催化剂催化效率的影响如下图。下列说法正确的是
的平衡转化率和催化剂催化效率的影响如下图。下列说法正确的是
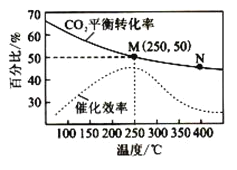
A.M点的正反应速率![]() 大于N点的逆反应速率v逆
大于N点的逆反应速率v逆
B.若投料比![]() ,则图中M点己烯的体积分数为
,则图中M点己烯的体积分数为![]()
C.![]() ,催化剂对
,催化剂对![]() 平衡转化率的影响最大
平衡转化率的影响最大
D.当温度高于![]() ,升高温度,平衡逆向移动导致催化剂的催化效率降低
,升高温度,平衡逆向移动导致催化剂的催化效率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在调节好pH和![]() 浓度的废水中加
浓度的废水中加![]() ,能氧化降解污染物。现用该方法降解污染物
,能氧化降解污染物。现用该方法降解污染物![]() ,控制
,控制![]() 、
、![]() 和
和![]() 的初始浓度相同,设计如下对比实验探究温度、pH对该降解反应速率的影响,测得
的初始浓度相同,设计如下对比实验探究温度、pH对该降解反应速率的影响,测得![]() 的浓度随时间变化的关系如下图。
的浓度随时间变化的关系如下图。
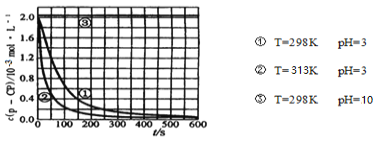
下列结论或推断不正确的是
A.实验①、②表明适当升高温度,降解反应速率增大
B.根据反应原理推断,温度过高,反而会使降解速率变慢
C.313K、![]() 时,在
时,在![]() 内,
内,![]() 的分解平均速率约为
的分解平均速率约为![]() mol/(L·s)
mol/(L·s)
D.室温下,实验过程中取样分析浓度可以采用迅速加碱调节溶液pH的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+,对于该平衡,下列叙述正确的是( )
CH3COO-+H+,对于该平衡,下列叙述正确的是( )
A.加入少量NaOH固体,平衡向正反应方向移动,溶液中c(H+)增大
B.加水,平衡向正反应方向移动,c(CH3COO-)和c(H+)增大
C.加入少量HCl,平衡逆向移动,溶液中c(H+)减少
D.加入少量CH3COONa固体,平衡向逆反应方向移动,溶液导电能力增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
|温度/ ℃ | 700 | 900 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K=____________,△H____0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。则6s时c(A)=_____mol·L-1, C的物质的量为______mol;若反应经一段时间后,达到平衡时A的转化率为_____,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为_________;
(3)判断该反应是否达到平衡的依据为______(填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
(4)1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为_____________。
A(g)+B(g)的平衡常数的值为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水的电离平衡曲线如图所示,下列说法正确的是

A.水的离子积常数关系为:KW(B)>KW(A)>KW(C)>KW(D)
B.向水中加入醋酸钠固体,可从C点到D点
C.B点对应的温度下,pH=4的硫酸与pH=10的氢氧化钠溶液等体积混合,溶液的pH=7
D.升高温度可实现由C点到D点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com