
具有下列电子排布式的原子中,半径最大的是( )
A.1s22s22p63s23p1 B.1s22s22p5
C.1s22s22p63s23p4 D.1s22s22p1
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A.Al3+、Cl-、AlO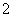 、SiO
、SiO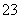
B.H+、Na+、S2-、ClO-
C.K+、Mg2+、SO 、MnO
、MnO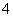
D.Fe3+、Ca2+、SCN-、NO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A.Na2S2O3溶液中加入稀硫酸:2S2O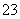 +2H+===SO
+2H+===SO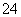 +3S↓+H2O
+3S↓+H2O
B.向NH4HSO3溶液中滴加少量KOH溶液:NH +OH-===NH3·H2O
+OH-===NH3·H2O
C.盐碱地(含较多NaCl、Na2CO3)中加入石膏,降低土壤的碱性,涉及的方程式为Ca2++CO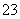 ===CaCO3↓
===CaCO3↓
D.在海带灰的滤液中加入几滴稀硫酸,再加入双氧水,能使淀粉溶液变蓝:2I-+H2O2+2H+===I2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
可以由下列反应合成三聚氰胺:CaO+3C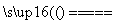 CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2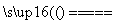 CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:_____________________________________________。
CaCN2中阴离子为CN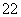 ,与CN
,与CN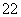 互为等电子体的分子有N2O和________(填化学式),由此可以推知CN
互为等电子体的分子有N2O和________(填化学式),由此可以推知CN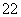 的空间构型为________。
的空间构型为________。
(2)尿素分子中C原子采取________杂化。尿素分子的结构简式是________。
 (3)三聚氰胺(
(3)三聚氰胺(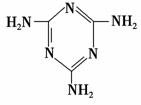 )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸(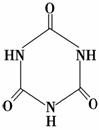 )后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
)后,三聚氰酸与三聚氰胺分子相互之间通过________结合,在肾脏内易形成结石。
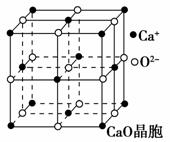
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为________。CaO晶体和NaCl晶体的晶格能分别为:CaO 3 401 kJ·mol-1、NaCl 786 kJ·mol-1。导致两者晶格能差异的主要原因是__________________________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
A.周期表中的主族都有非金属元素
B.周期表中的主族都有金属元素
C.周期表中的非金属元素都位于短周期
D.周期表中的过渡元素都是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D都是短周期元素。A的原子核外有两个电子层,最外层已达到饱和。B位于A元素的下一周期,最外层的电子数是A最外层电子数的1/2。C的离子带有两个单位正电荷,它的核外电子排布与A元素原子相同。D与C属同一周期,D原子的最外层电子数比A的最外层电子数少1。
(1)根据上述事实判断:A是________,B是________,C是________,D是________。
(2)C的离子的核外电子排布式为________________;D原子的核外电子排布式为______________。
(3)B位于第________周期________族,它的最高价氧化物的化学式是__________,最高价氧化物的水化物是一种________酸。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com