
【题目】常温下,用0.1 mol/L的HCl溶液滴定a mL NaOH稀溶液,反应恰好完全时,消耗HCl溶液b mL,此时溶液中氢氧根离子的浓度c(OH-)是( )
A. 1×10-7 mol/L B. 1×107 mol/L C. 0.1mol/L D. 0.01 mol/L
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】化学反应的本质是旧化学健的断裂和新化学键的形成。已知某些化学键的键能数据如下:
化学键 | H—H | Cl—Cl | H—Cl |
键能/(kJ·mol-1) | 436 | 243 | 431 |
则下列热化学方程式不正确的是( )
A. ![]() H2(g)+
H2(g)+![]() Cl2(g)===HCl(g)
Cl2(g)===HCl(g)
ΔH=-91.5 kJ·mol-1
B.H2(g)+Cl2(g)===2HCl(g) ΔH=-183 kJ·mol-1
C. ![]() H2(g)+
H2(g)+![]() Cl2(g)===HCl(g)
Cl2(g)===HCl(g)
ΔH=+91.5 kJ·mol-1
D.2HCl(g)===H2(g)+Cl2(g) ΔH=+183 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现某药物M能治疗心血管疾病是因为它在人体内能释放出一种“信使分子”D,并阐明了D在人体内的作用原理。为此他们荣获了1998年诺贝尔生理学或医学奖。
请回答下列问题:
(1)已知M的相对分子质量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%。则M的分子式是______________。D是双原子分子,相对分子质量为30,则D的分子式为______________。
(2)油脂A经下列途径可得到M。

图中②的提示: ![]()
反应①的反应类型是_________________。 反应②的化学方程式是 ________________。
(3)C是B和乙酸在一定条件下反应生成的化合物,分子量为134,写出C一种可能的结构简式:________________________________。
(4)若将0.15 mol B与足量的金属钠反应,则需消耗___________g金属钠。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请参考题中图表,已知E1=134 kJ·mol-1、E2=368 kJ·mol-1,根据要求回答下列问题:
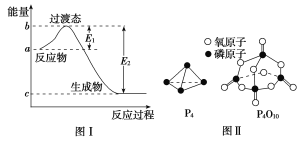
(1)图Ⅰ是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________(填“增大”“减小”或“不变”,下同),ΔH的变化是__________________________。
请写出NO2和CO反应的热化学方程式:______________________________。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g)
ΔH=+49.0 kJ·mol-1
②CH3OH(g)+![]() O2(g)===CO2(g)+2H2(g)
O2(g)===CO2(g)+2H2(g)
ΔH=-192.9 kJ·mol-1
又知③H2O(g)===H2O(l) ΔH=-44 kJ·mol-1,则甲醇蒸汽燃烧为液态水的热化学方程式为______________________________。
(3)下表所示是部分化学键的键能参数:
化学键 | P—P | P—O | O===O | P===O |
键能/(kJ·mol-1) | a | b | c | x |
已知白磷的燃烧热为d kJ·mol-1,白磷及其完全燃烧的产物的结构如图Ⅱ所示,则表中x=________kJ·mol-1(用含a、b、c、d的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是

A. 铜电极上发生氧化反应
B. 电池工作一段时间后,甲池的c(SO42-)减小
C. 电池工作一段时间后,乙池溶液的总质量增加
D. 阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )

A. 丙与戊的原子序数相差28
B. 气态氢化物的稳定性:庚<己<戊
C. 常温下,庚和乙形成的化合物易溶于水
D. 丁的最高价氧化物不与任何酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2CrO![]() +2H+Cr2O
+2H+Cr2O![]() +H2O。某科研小组用如图电解装置,由Na2CrO4溶液制取Na2Cr2O7溶液。下列有关叙述正确的是( )
+H2O。某科研小组用如图电解装置,由Na2CrO4溶液制取Na2Cr2O7溶液。下列有关叙述正确的是( )

A.CrO![]() 生成Cr2O
生成Cr2O![]() 的反应为非氧化还原反应,不能通过电解方法获得
的反应为非氧化还原反应,不能通过电解方法获得
B.a为电源正极
C.d口流出的NaOH溶液的浓度与c口通入的NaOH溶液的浓度相同
D.Na+从右侧通过阳离子交换膜进入左侧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。下列有关叙述不正确的是
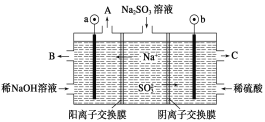
A.图中a极连接电源的负极
B.A口放出的物质是氢气,C口放出的物质是氧气
C.b极电极反应式为:SO32--2e-+H2O===SO42-+2H+
D.电解过程中阴极区碱性明显增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F、G、H八种短周期主族元素,原子序数依次增大。A是所有元素中原子半径最小的元素。B、C、D同周期且相邻,C的气态氢化物的水溶液显碱性。E是同周期元素中金属性最强的元素。F的氧化物既能溶于强酸又能溶于强碱。G的一种氧化物能使品红溶液褪色,且G原子的M层电子数是K层电子数的3倍。按要求回答下列向题:
(1) C元素在周期表中位置_________;F原子的原子结构示意图是________。
(2)E与D形成的化合物E2D2的电子式是_______;B与D形成的化合物BD2的结构式是_____。
(3)B、G、H三种元素最高价氧化物的水化物的酸性从强到弱的顺序是________。E所在的周期中离子半径最小的是________。(用相应酸的化学式或离子符号回答问题)
(4)G的一种氧化物能使酸性高锰酸钾溶液褪色,对应的离子方程式_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com