
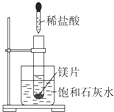
 如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入一小块镁片,再用滴管滴入10mL 0.2mol/L的稀盐酸于试管中,测得生成氢气在标况的体积为11.2mL后反应停止,同时观察到盛饱和石灰水的烧杯中出现浑浊的现象.请回答下列问题:
如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入一小块镁片,再用滴管滴入10mL 0.2mol/L的稀盐酸于试管中,测得生成氢气在标况的体积为11.2mL后反应停止,同时观察到盛饱和石灰水的烧杯中出现浑浊的现象.请回答下列问题:分析 (1)放热反应中反应物总能量大于生成物总能量;
(2)发生反应:Mg+2H+=Mg2++H2↑;根据氢气结合化学方程式计算消耗盐酸的物质的量,根据C=$\frac{n}{V}$计算剩余氢离子浓度,再根据pH=-lgc(H+)计算溶液pH;
(3)单质、气体、沉淀等写化学式,可溶性强电解质写离子.
解答 解:(1)放热反应中反应物总能量大于生成物总能量,该反应是放热反应,所以MgCl2溶液和H2的总能量低于镁片和盐酸的总能量,故答案为:低于;(2)由Mg+2H+=Mg2++H2↑,生成氢气为$\frac{11.2×10{\;}^{-3}}{22.4}$=0.0005mol,则剩余盐酸浓度为即c(H+)=$\frac{0.2×10×10{\;}^{-3}-0.0005×2}{10×10{\;}^{-3}}$=0.1mol/L,
故pH=-lg0.1=1,
故答案为:1;
(3)单质、气体、沉淀等写化学式,可溶性强电解质写离子,离子方程式为Mg+2H+=Mg2++H2↑,故答案为:Mg+2H+=Mg2++H2↑.
点评 本题以镁、氢氧化钙为载体考查能量守恒、离子方程式的书写等知识点,明确实验原理是解本题关键,注意分析氢氧化钙溶液变化,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Na+、H+、AlO2-、C1- | B. | ClO-、K+、OH一、HSO3- | ||
| C. | K+、Na+、SiO32-、SO42一 | D. | K+、A13+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某温度时,在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
某温度时,在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加入盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加入盐酸白色沉淀消失,一定有Ba2+ | |
| D. | 某溶液中加入氢氧化钠溶液生成蓝色沉淀,一定有Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 名称 | 托盘天平 (带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9:8 | B. | 11:12 | C. | 12:11 | D. | 3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| C. | 向FeBr2溶液中通入足量 Cl2:2Fe2++2Br-+2Cl2═Br2+2Fe3++4Cl- | |
| D. | 向50 mL 1 mol•L-1明矾溶液中滴入两滴0.1 mol•L-1Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com