
下列关于有机物的叙述正确的是
A.甲苯分子中所有原子均在同一个平面上
B.乙烯使KMnO4溶液褪色,是因为两者发生了加成反应
C.分子式为C4H9Br的同分异构体共有4种(不考虑立体异构)
D.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源:2013-2014山西省5月月考高二化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.乙酸与碳酸钠溶液反应:2H++CO32—== CO2↑+H2O
B.醋酸溶液与新制氢氧化铜反应:CH3COOH+OH- → CH3COO-+H2O
C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O → 2C6H5OH+CO32—
D.甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH-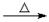 CO32—+2NH4++4Ag↓+6NH3+2H2O
CO32—+2NH4++4Ag↓+6NH3+2H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014山西忻州一中、长治二中、临汾一中、康杰中学高三化学(解析版) 题型:选择题
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-,横坐标表示加入NaOH的体积)。根据图示判断,下列说法正确的是
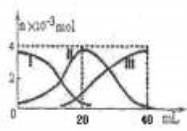
A.当V(NaOH)=40mL时,c (Na+)+ c(H+)=2 c(A2-)+c(OH-)
B.当V(NaOH)=20mL时,溶液中离子浓度大小关系: c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.滴加过程中当溶液呈中性时,V(NaOH)<20mL
D.HA-的电离程度小于水解程度
查看答案和解析>>
科目:高中化学 来源:2013-2014山西大学附中高三第二学期5月理科综合化学试卷(解析版) 题型:选择题
硫酸亚铁是一种重要的化工原料,可以制备多种物质。有关下列制备方法错误的是
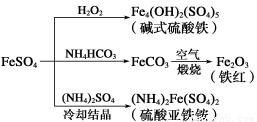
A.制备碱式硫酸铁利用了过氧化氢的氧化性
B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D.制备(NH4)2Fe(SO4)2利用了它的溶解度比FeSO4的溶解度大这一性质
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省青岛市高三第二次模拟考试理综化学试卷(解析版) 题型:简答题
(16分)复方过氧化氢消毒剂具有高效、环保、无刺激无残留,其主要成分H2O2。
(1)H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了甲、乙两种实验装置。
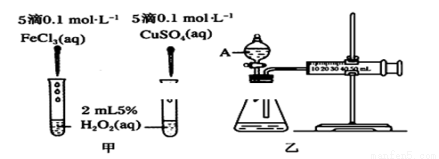
若利用甲实验,可通过观察________现象,从而定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是________;若利用乙实验可进行定量分析,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是________。
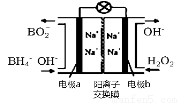
(2)在含有表面活性剂的酸性水溶液中,以碳为电极,通直流电进行电解可制取氢气和过氧化氢,过氧化氢在 (填“阴极”、“阳极”)产生。
以H2O2和硼氢化合物NaBH4(B的化合价为+3价)作原料的燃料电池,可用作通信卫星电源。其工作原理如图所示,写出a极上的电极反应式: ,正极材料采用MnO2,MnO2除了作电极材料之外还可能具有的作用为
(3)锗(Ge)与碳是同主族元素,最新研究表明有机锗具有明显的抗肿瘤活性,锗不与NaOH 溶液反应,但在有H2O2存在时可与NaOH 溶液反应生成锗酸盐,其化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省烟台市高三5月适应性测试一理综化学试卷(解析版) 题型:填空题
(12分):【化学——物质结构与性质】
A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大。B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族。B、C、D的最高价氧化物的水化物均能互相反应生成盐和水,D的原子半径是同周期原子中最小的。
根据以上信息,回答下列问题:
(1)上述A、B、C、D四种元素中第一电离能最小的是 ,电负性最大的是 , 原子半径由小到大的顺序为 。 (填相关元素的元素符号)
(2)A和D的氢化物中,沸点较高的是 (填相关物质的分子式);其原因是 。
(3)A和E可形成离子化合物,其晶胞结构如图所示:则每个晶胞中含阳离子的数目为 ,含阴离子的数目为 ,该离子化合物的化学式为 。

查看答案和解析>>
科目:高中化学 来源:2013-2014山东省烟台市高三5月适应性测试一理综化学试卷(解析版) 题型:选择题
利用实验器材(规格和数量不限)能完成相应实验的一项是
选项 | 实验器材(省略夹持装置) | 相应实验 l |
A | 三脚架、泥三角、坩埚、坩埚钳 | 用CuSO4 |
B | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用浓盐酸配制0.1mol·L-1的HCl溶液 |
C | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸和乙醇 |
D | 烧杯、酸式滴定管、碱式滴定管 | 用H2SO4标准液滴定未知浓度的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省潍坊市下学期期中考试高二化学试卷(解析版) 题型:推断题
(14分) 有机物A1和A2分别和浓硫酸在一定温度下共热只生成烃B,B的蒸气密度是同温同压下H2密度的59倍,在催化剂存在下,1mol B可以和4mol H2发生加成反应,B的一元硝化产物有三种(同种类型)。有关物质之间的转化关系(其中F的分子式为C9H10O3)如下:
有机物A1和A2分别和浓硫酸在一定温度下共热只生成烃B,B的蒸气密度是同温同压下H2密度的59倍,在催化剂存在下,1mol B可以和4mol H2发生加成反应,B的一元硝化产物有三种(同种类型)。有关物质之间的转化关系(其中F的分子式为C9H10O3)如下:
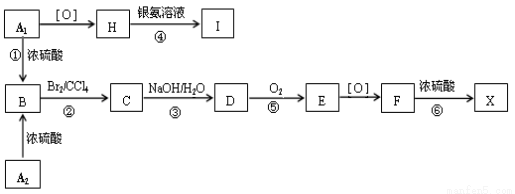
请回答下列问题:
(1) 反应① ~ ⑥中属于取代反应的是:_______________。
(2) 写出A2和F两物质的结构简式:A2 ______________;F_____________________。
(3) 写出③、④两步反应的化学方程式:
_______________________________________________________________。
_______________________________________________________________。
(4) 化合物E有多种同分异构体,其中属于酯类且具有两个对位侧链的同分异构体的结构简式:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com