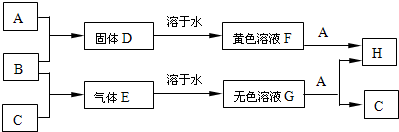
解:B是黄绿色气体,故B是氯气,A和B生成D,D是氯化物,D溶于水得黄色溶液,D含有铁离子,则D是氯化铁,A是铁,氯化铁和铁反应生成氯化亚铁,则H是氯化亚铁,氯气和C反应生成E,E溶于水得无色溶液G,G和铁反应生成氯化亚铁和C,根据元素守恒知,G是盐酸,C是氢气,E是氯化氢.
(1)通过以上分析知,B是Cl
2,氢气在氯气中燃烧现象是:安静燃烧,发出苍白色火焰;
故答案为:Cl
2,安静燃烧,发出苍白色火焰;
(2)铁在氯气中燃烧生成氯化铁,反应方程式为2Fe+3Cl
2
2FeCl
3,铁和铁离子反应生成亚铁离子,离子方程式为
Fe+2Fe
3+=3Fe
2+;
故答案为:2Fe+3Cl
2
2FeCl
3,Fe+2Fe
3+=3Fe
2+;
(3)氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,离子方程式为:Cl
2+2OH
-=Cl
-+ClO
-+H
2O;
故答案为:Cl
2+2OH
-=Cl
-+ClO
-+H
2O;
(4)F、G、H三种溶液中所含的相同阴离子是Cl
-,氯离子和硝酸酸化的硝酸银反应生成白色沉淀,氯离子的检验方法是:先用稀硝酸酸化,再滴加硝酸银溶液,若产生白色沉淀,则原溶液中含有氯离子;
故答案为:Cl
-,先用稀硝酸酸化,再滴加硝酸银溶液,若产生白色沉淀,则原溶液中含有氯离子.
分析:B是黄绿色气体,故B是氯气,A和B生成D,D是氯化物,D溶于水得黄色溶液,D含有铁离子,则D是氯化铁,A是铁,氯化铁和铁反应生成氯化亚铁,则H是氯化亚铁,氯气和C反应生成E,E溶于水得无色溶液G,G和铁反应生成氯化亚铁和C,根据元素守恒知,G是盐酸,C是氢气,E是氯化氢.
点评:本题以元素化合物的推断为载体考查了元素化合物的性质,能正确推断元素化合物是解本题的关键,注意氯离子的检验是高考的热点,铁在氯气中燃烧时,无论铁是否过量都生成氯化铁,为易错点.

 2FeCl3,铁和铁离子反应生成亚铁离子,离子方程式为
2FeCl3,铁和铁离子反应生成亚铁离子,离子方程式为 2FeCl3,Fe+2Fe3+=3Fe2+;
2FeCl3,Fe+2Fe3+=3Fe2+;

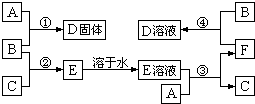 (2009?福清市模拟)室温下,单质A、B、C分别为固体、黄绿色气体、无色气体.在合适反应条件下,它们可以按下面框图进行反应;又知单质A是当今世界产量最大的金属,E的溶液是无色的.请回答:
(2009?福清市模拟)室温下,单质A、B、C分别为固体、黄绿色气体、无色气体.在合适反应条件下,它们可以按下面框图进行反应;又知单质A是当今世界产量最大的金属,E的溶液是无色的.请回答:

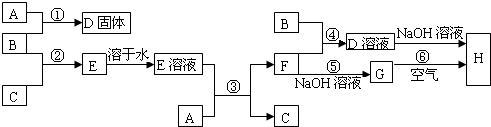
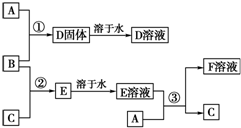 室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按如图所示进行反应.又知E溶液是无色的,F溶液是浅绿色的.请回答:
室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按如图所示进行反应.又知E溶液是无色的,F溶液是浅绿色的.请回答: