
 ,在B分子中Y原子的杂化方式为sp3,B中O-Y-H的键角小于(填“大于”“等于”或“小于”)A中O-Y-H键角.
,在B分子中Y原子的杂化方式为sp3,B中O-Y-H的键角小于(填“大于”“等于”或“小于”)A中O-Y-H键角. 分析 Y原子的L层p轨道中有2个电子1s22s22p2,为6号元素碳;Z原子的L电子层中,有三个未成对的电子,且无空轨道,所以Z是氮;E原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1,1s22s22p63s23p63d104s2,30号锌元素,XYZ分子中的三个原子除X原子外最外层均为8电子构型,所以X是氢,以此解答该题.
解答 解:Y原子的L层p轨道中有2个电子1s22s22p2,为6号元素碳;Z原子的L电子层中,有三个未成对的电子,且无空轨道,所以Z是氮;E原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1,1s22s22p63s23p63d104s2,30号锌元素,XYZ分子中的三个原子除X原子外最外层均为8电子构型,所以X是氢,
(1)HCN分子中的三个原子除H原子外均为8电子构型,C原子形成4个共价键、N原子形成3个共价键,则HCN分子的结构式为H-C≡N,共价单键为σ键,共价三键中一个是σ键两个是π键,所以氢氰酸分子中含有两个σ键两个π键,
故答案为:σ键、π键;
(2)NH3分子是一种常见气体,氨气分子中N原子价层电子对个数是4,所以N原子采用sp3杂化;氢键的存在增大氨气的溶解性,
故答案为:sp3;氨气与氨气、氨气和水分子之间均易形成氢键;
(3)E2+为Zn2+,Zn是30号元素,失去最外层2个电子的核外电子排布式是 1s22s22p63s23p63d10,故答案为:1s22s22p63s23p63d10;
(4)在B分子中Y原子形成4个δ键,为sp3杂化,B中O-Y-H的键角约为109028',而B中O-Y-H的键角为1200,B中O-Y-H的键角小于A中O-Y-H键角,
故答案为:sp3;小于.
点评 本题考查元素的推断以及分子杂化方式、分子构型、离子核外电子排布等,为高频考点,侧重考查学生分析问题、运用知识解决问题能力,会利用价层电子对互斥理论、构造原理等知识点解答,综合性较强.


科目:高中化学 来源: 题型:选择题
| A. | 同分异构体 | B. | 不同密度的核素 | C. | 同位素 | D. | 同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大反应物的量,化学反应速率一定加快 | |
| B. | 气体反应体系的压强增大,化学反应速率一定加快 | |
| C. | 与金属锌反应时,硫酸的浓度越大,产生H2速率越快 | |
| D. | 2molX气体在2L的容器中反应,4s后浓度变为0.5mol•L-1,则其反应速率为0.125mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 化学键 | H-H | O-O | O═O | O-H |
| 能量(kJ) | 436 | 138 | 498 | 465 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 已知X、Y、Z三元素的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.C、D是由X、Y、Z中两种元素组成的化合物,C通常状况下为无色液体,D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板.各物质之间的转换关系如图,部分生成物省略.
已知X、Y、Z三元素的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.C、D是由X、Y、Z中两种元素组成的化合物,C通常状况下为无色液体,D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板.各物质之间的转换关系如图,部分生成物省略.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
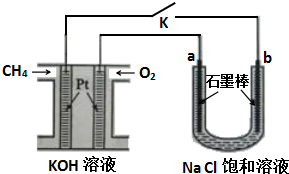
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com