
(10分)某研究小组为了研究不同条件下金属铝粉在过量稀硫酸中的溶解性能,设计如下实验。已知:c(H2SO4)=4.5 mol·L-1,反应均需要搅拌60min。
编号 | 温度/℃ | 加入某盐 | H2SO4体积/mL | H2O体积/mL | 铝粉加入量/g | 铝粉溶解量 /g |
① | 20 | 不加 | 40 | 0 | 2.0050 | 0.0307 |
② | 80 | 不加 | 40 | 0 | 2.0050 | 0.1184 |
③ | t1 | 不加 | 20 | V1 | 2.0050 | ﹨ |
④ | t2 | 5 mL0.01 mol·L-1 CuSO4溶液 | 20 | V2 | 2.0050 | ﹨ |
(1)实验①和②的目的是 。
为了获得铝粉溶解量,还需要测量的数据是 。
(2)实验①和③是为了研究硫酸的浓度对该反应的影响,则t1= ℃,V1= mL。
(3)实验③和④是为了研究加入CuSO4溶液对该反应的影响,则t2= ℃,V2= mL。
研究表明,在相同条件下加入少量CuSO4有利于Al的溶解。原因是 。
(1)其它条件不变,温度对稀硫酸溶解铝粉量的影响。 (2分)
反应60min后剩余铝粉的质量 (2分)
(2)20 ;20 (2分,各1分)
(3)20 ;15 (2分,各1分)
加入硫酸铜,铝置换出少量的铜构成铝铜原电池,加快反应速率。(2分)
【解析】
试题分析:⑴实验①和②的实验温度不同,目的是探究温度对稀硫酸溶解铝粉量的影响;由总质量减去剩余铝粉的质量可确定溶解量;
⑵实验①和③是为了研究硫酸的浓度对该反应的影响,则温度应相同(20℃),但浓度不同,根据总体积相同,则V1=20mL;
⑶实验③和④是为了研究加入CuSO4溶液对该反应的影响,则温度、浓度应相同,因加入5mL 0.01mol?L-1CuSO4溶液,则加水的体积应为15mL,加入硫酸铜,铝置换出铜,可形成铝、铜原电池反应,从而加快反应速率。
考点:考查化学反应速率的影响的因素。


科目:高中化学 来源:2014高考名师推荐化学--预测1 题型:简答题
工业上常用铁质容器盛装冷浓硫酸,为研究铁质材料与热浓硫酸的反应,某学校学习小组进行以下探究实验:
[一](1)将已除去表面氧化物的铁钉(碳素钢)放入冷的热的浓硫酸中,10分钟后移人硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是 ;
(2)另称取铁钉6.0g放入15.0mL浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。①甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用
(选填序号)
a.KSCN溶液和氯水 .b铁.粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取336mL(标准状况)气体Y通入足量溴水中,发生反应SO2+Br2+2H2O═2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g由于此推知气体Y中SO2的体积分数为 ;
[探究二]分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和Q气体,为此设计了下列探究实验装置(图中夹持仪器省略)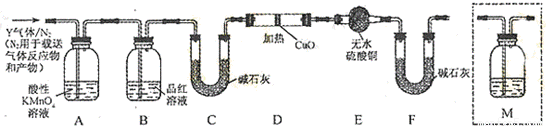
(3)装置B中试剂的作用是 ;
(4)认为气体Y中还含有Q的理由是 ;(用化学方程式表示)
(5)为确认Q的存在,需在装置中添加M于 (选填序号)
a.A之前 b.A-B间 c.B-C间 d.C-D间
(6)如果气体Y中含有H2,预计实验的现象应是 ;
(7)若要测定限定体积气体Y中H2含量(标准状况下约有28ml H2),除用测量H2体积方法外,否选用质量称量方法?做出判断并说明理由 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学--线索综合1 题型:简答题
A、B、C、D、E、F六种元素,其中A、B、C、D、E为短周期主族元素。它们之间的关系如下:
Ⅰ.原子半径:A < C< B < E< D
Ⅱ.原子的最外层电子数:A=D C=E A + B=C
Ⅲ.原子的核外电子层数:B=C=2A
Ⅳ.B元素的主要化合价:最高正价+最低负价=2
请回答:
(1)甲为由A、B两种元素组成的常见气体,写出其电子式 ;
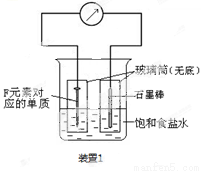
(2)写出某黑色含F的磁性氧化物与E最高价氧化物对应水化物的稀溶液反应的离子方程式 。装置1经过一段时间向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 。单质F发生 (填电化学腐蚀类型)
(3)向A、B、C三种元素组成的某盐稀溶液中滴加AgNO3溶液生成白色沉淀,该反应的化学方程式为 ,已知该盐溶液常温下呈酸性,则0.1mol/L该盐溶液中离子浓度的大小顺序为 。
(4)上述元素中的五种元素可形成一种常见复盐,经检测该复盐中三种离子的个数比为2:1:2,则该复盐的化学式为 。为检验该复盐中的某种有色离子存在,请写出实验的操作步骤和现象 。
查看答案和解析>>
科目:高中化学 来源:2014福建安溪一中、养正中学、惠安一中高一下学期期末化学试卷(解析版) 题型:选择题
已知某反应aA(g)+bB(g)?==?cC(g)的各物质浓度数据如下:
| A | B | C |
起始浓度(mol·L-1) | 3.0 | 1.0 | 0 |
2 s末浓度(mol·L-1) | 1.8 | 0.6 | 0.8 |
据此可推算出a∶b∶c是( )
A.9∶3∶4 B.3∶1∶2 C.2∶1∶3 D.3∶2∶1
查看答案和解析>>
科目:高中化学 来源:2014福建安溪一中、养正中学、惠安一中高一下学期期末化学试卷(解析版) 题型:选择题
下列各组顺序的排列不正确的是( )
A.原子半径:Na > Mg > Al > H B.热稳定性: HCl < H2S < PH3
C.酸性强弱:H2SiO3 < H2CO3 < H3PO4 D.氧化性:K+ < Na+ < Mg2+ < Al3+
查看答案和解析>>
科目:高中化学 来源:2014江苏常熟市高二化学期末模拟4(必修2、选修4、结构)试卷(解析版) 题型:选择题
下列实验现象与对应结论均正确的是
选项 | 操作 | 现象 | 结论 |
A | SO2水溶液中滴加盐酸酸化的BaCl2溶液 | 产生白色沉淀 | BaSO3难溶于盐酸 |
B | Al放入浓HNO3中 | 无明显现象 | Al表面被浓HNO3氧化形成致密的氧化膜 |
C | Na2SiO3溶液中通入CO2气体 | 产生白色胶状沉淀 | H2SiO3的酸性比H2CO3的酸性强 |
D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
查看答案和解析>>
科目:高中化学 来源:2014江苏常熟市高二化学期末模拟4(必修2、选修4、结构)试卷(解析版) 题型:选择题
下列说法不正确的是
A.Na2O2能与CO2反应,可用作呼吸面具的供氧剂
B.Al2O3熔点高,可用于制作耐高温仪器
C.明矾能水解生成Al(OH)3胶体,可用作净水剂
D.SiO2有导电性,可用于制备光导纤维
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版4.3铜及其化合物 金属材料与复合材料练习卷(解析版) 题型:选择题
某地污水中含有Zn2+、Hg2+、Fe3+、Cu2+四种阳离子。甲、乙、丙三位同学设计的从该污水中回收金属铜的方案如下:
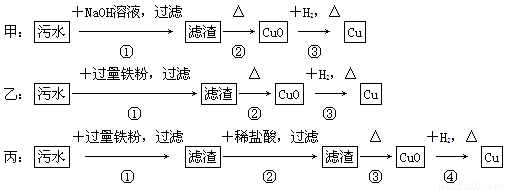
下列判断正确的是( )。
A.三种实验方案都能制得纯净的铜
B.乙方案中加过量铁粉可以将四种阳离子全部还原
C.甲方案中的反应涉及置换、分解、化合、复分解四种反应类型
D.丙方案会产生环境污染
查看答案和解析>>
科目:高中化学 来源:2014年高考化学鲁科版3.3硫的转化练习卷(解析版) 题型:选择题
2012年3月13日,一艘运载7 000吨浓硫酸的韩国籍货船在汕尾海域发生自沉,船上18名外籍船员被救起。下列有关说法正确的是( )。
A.浓硫酸易挥发,从沉船中抽出的浓硫酸要密封保存
B.抽出的浓硫酸有很强的氧化性,不能直接保存在铁制容器中
C.在打捞时,如果盛装浓硫酸的舱室内进水,可能会发生爆炸
D.硫酸工业尾气虽然无害,但它的过度排放会造成温室效应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com