
����Ŀ�����ӹ�ҵ����30%��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ��������ӡˢ��·�塣
(1)д��FeCl3��Һ�����ͭ������Ӧ�Ļ�ѧ����ʽ:______________________��
(2)ij����ʦΪ�˴�ʹ�ù��ĸ�ʴ��Һ����Ҫ��CuCl2��FeCl3��Һ�ȣ��л���ͭ�������»�ô�����FeCl3��Һ����������ͼ��ʾ����:����֪���ӹ�����ΪFe���ӹ�����Ϊϡ���ͨ����ΪCl2��
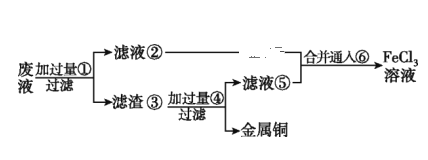
������ʵ��������������Ҫ����Ϊ___________________���ѧʽ����д�����ڢ��ĺϲ�Һ��ͨ���������ӷ���ʽ:______________________________��
�����Ʋ�����FeCl2��Һʱ���������м����Ŀ����_______________________________��
��Ҫ֤��FeCl3��Һ�Ƿ���Fe2+����ѡ������ѡ���е�______________����֪����������ʺ�������ɫ��������
A������ K3[Fe(CN)6]��Һ ��B������NaOH��Һ C������KSCN��Һ
(3)����1.2 L��3 mol FeCl2��������Һǡ����0.6 mol HIO3��ȫ��Ӧ����ԭ����Ϊ_______���ѧʽ����֪��������������Һ���������÷�Ӧ���ӷ���ʽΪ___________________________________��
���𰸡�Cu��2Fe3����Cu2����2Fe2�� Cu��Fe Cl2��2Fe2����2Fe3����2Cl�� ��ֹFe2����������2Fe3����Fe��3Fe2�� A I2 12H+��10Fe2����2IO3����10Fe3����I2��6H2O�� 10H+��10Fe2����2HIO3��10Fe3����I2��6H2O
��������
(1) ͭ���Ȼ�����Ӧ�����Ȼ�ͭ���Ȼ�������
(2) ��Ӧ�к����Ȼ��������Ȼ�ͭ���ɹ������̿�֪���������к��н���ͭ����Ӧ�Ƿ�Һ�������Fe��Ӧ����Һ���к����Ȼ�������ͨ���������Եõ��Ȼ������������к��н���ͭ��δ��Ӧ�������������ᣬ���ˣ�����ͭ����Һ���к����Ȼ�����������Һ�ںϲ����Ʊ��Ȼ������ݴ˽��н��
(3) ��I2����Һ��������Һ��������1.2 L��3 mol FeCl2����Һǡ����0.6 mol HIO3��ȫ��Ӧ����I2��ͬʱ��������������ΪFe3+����������غ㣬��Ӧ��ˮ���ɣ��ݴ�д��������Ӧ�����ӷ���ʽ��
(1) ͭ���Ȼ�����Ӧ�����Ȼ������Ȼ���������Ӧ����ʽΪ��2FeCl3+Cu�T2 FeCl2+CuCl2��
(2) �ɹ������̿�֪���������к��н���ͭ��Ŀ������ȡ�Ȼ�������ҺӦ������������Fe��Ӧ���ʢ�Fe����Һ���к���FeCl2��ͨ����������Եõ��Ȼ������������к��н���Cu��δ��Ӧ��Fe����������ᣬ���ˣ�����ͭ����Һ���к���FeCl2������Һ�ںϲ����Ʊ��Ȼ�����������������֪����Fe ��FeCl2��Fe��Cu ��HCl ��FeCl2��Cl2��
��ʵ�����������к��н���Cu��δ��Ӧ��Fe����ڢݵĺϲ�Һ��ͨ��ķ�Ӧ���������������������������ӣ���Ӧ�����ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-��
��Fe2+���ӱ�������Ϊ�������е�����������Ϊ�� Fe3+�����Դ�ʱ�������ۣ�����Ϊ���ܽ����ɵ�Fe3+��ԭΪFe2+�����������ӷ�ӦΪ2Fe3++Fe�T3Fe2+��
���ں���Fe2+����Һ�еμ�K3[Fe(CN)6]��Һ������ɫ�������ɣ������Fe2+Ӧѡ��K3[Fe(CN)6]��Һ���ʴ�ΪA��
(3) ��I2����Һ��������Һ��������1.2 L��3 mol FeCl2����Һǡ����0.6 mol HIO3��ȫ��Ӧ����I2��ͬʱ��������������ΪFe3+����������غ㣬��Ӧ��ˮ���ɣ��ݴ�д��������Ӧ�����ӷ���ʽΪ12H+��10Fe2����2IO3����10Fe3����I2��6H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���谢���ӵ�����ΪNA��������˵����ȷ����
A.��ҵ�ϳɰ�ÿ����NA��N��N����ͬʱ����3NA��N-H������Ӧ�ﵽƽ��
B.���³�ѹ�£�16g���������е�ԭ����ĿΪNA
C.��״���£�2.24L������ȼ�պ����ɵ�CO2�����Ϊ11.2 L
D.�����£�CH4����ȡ����Ӧ����1molCH2Cl2��������Ҫ����2NA��Cl2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijˮ��Һ�п��ܺ���Na����Al3����Fe3����Mg2����Ba2����NH4+��Cl����SO42-�����е������֡�ijͬѧȡ200 mL����Һ�ֳ����ȷ����ν�������ʵ�飺�����һ����Һ�мӹ�����NaOH��Һ����ȣ���ַ�Ӧ������0.02 mol����(���)������������ͬʱ�õ���Һ�ף�������Һ����ͨ�������CO2����ַ�Ӧ���ɰ�ɫ���������������ˡ�ϴ�ӡ����������صõ�1.02 g���壻����ڶ�����Һ�м���������BaCl2��Һ����ַ�Ӧ���ɰ�ɫ������������������ϴ�ӡ�����õ�11.65 g���塣�ݴˣ���ͬѧ�õ��Ľ�����ȷ����(����)
A. ʵ����в���������Ϊ���������ɵ�ԭ��Һ��c(NH4+)��0.02 mol/L
B. ʵ����еij�����һ����BaSO4��������Mg(OH)2
C. ��Ҫȷ��ԭ��Һ���Ƿ���Cl�����������������ʵ����֤
D. ԭ��Һ��һ������Na������c(Na��)��0.2 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�������A��B��C������ס��ҡ����Լ�����D��E��F��G��H������֮����ת����ϵ��ͼ��ʾ(ͼ����Щ��Ӧ��������ͷ�Ӧ������û�б��)����ʾ:�ƾvɫ��������������

��ش��������⣺
(1)д���������ʵĻ�ѧʽ��B______����______��H______��
(2)����Ҫ��ش�
��D��Һ��F��Һ�ڿ����л�ϵ�����_______��
�ڷ�Ӧ�����ӷ���ʽ________��
�۷�Ӧ�����ӷ���ʽ________��
�ܷ�Ӧ��ѧ����ʽ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A.�ھƾ��Ƽ��������£�Na2CO3��NaHCO3���嶼�ܷ����ֽ�
B.Cl2��һ���ж����壬������������ˮ��ɱ������
C.SiO2���ܺ�NaOH��Һ��Ӧ���ܺ�����ᷴӦ������������������
D.Na2SiO3ˮ��Һ�׳�ˮ���������Ʊ��轺��ľ�ķ�����ȵ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��.ij��ȤС�����10.0 g�������ޣ���90%��Al��������������Fe��Mg�����ʣ��Ʊ�����[KAl(SO4)2��12H2O]��ʵ��������ͼ��

��1���Լ���Ӧѡ��________������ĸ����
a.���� b.H2SO4��Һ c.��ˮ d.NaOH��Һ
��2���������ܽ��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ__________________________��
��3������ҺC�еõ�������ʵ�����Ϊ________��________�����ˣ�����ͼ��ʾװ�ý��иò��������е�һ����Ҫ������______________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С���ͬѧ��ѧϰ�˵绯ѧ���֪ʶ������ͼװ�ý���ʵ�飬��ش��������⣺
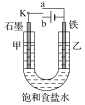
(1)ʵ��һ��������K��a���ӣ�����Ϊ_____�����缫��ӦʽΪ______��
(2)ʵ��һ�������о�С���ͬѧ�������ҵ缫�����϶����н����е�һ���Է�ֹ������ʴ����ȷ��ѡ����____(����ĸ���)��
A��Cu�� ��B��Zn���� C��Sn�� �� D��Ag
(3)ʵ���������K��b���ӣ�����__�����ܷ�Ӧ�����ӷ���ʽΪ______��
(4)����ʵ���������˵����ȷ����____(����ĸ���)��
A����Һ��Na������ƶ�
B���Ӽ����ݳ���������ʹʪ��ĵ��ۣ�KI��ֽ����
C����Ӧһ��ʱ������������ɻָ������ǰ����ʵ�Ũ��
D����Ӧ�ڽ����缫���ҵ缫���ռ������������һ�����
(5)���о�С���ͬѧ�ڽ���ʵ�����������Һ�еμӷ�̪��Һ������________(����������������)��������졣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£������������Ϊ 1.0 L �ĺ����ܱ������з�����Ӧ��2CH3OH(g)![]() CH3OCH3(g)��H2O(g)
CH3OCH3(g)��H2O(g)
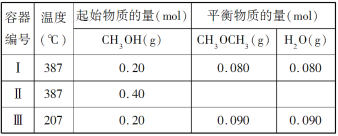
����˵����ȷ���ǣ� ��
A.�÷�Ӧ������ӦΪ���ȷ�Ӧ
B.�ﵽƽ��ʱ���������е� CH3OH ����������������е�С
C.�������з�Ӧ����ƽ������ʱ����������еij�
D.����ʼʱ���������г��� CH3OH 0.15 mol��CH3OCH3 0.15 mol �� H2O 0.10 mol����Ӧ�� ������Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. �����ܽ�ˮ���е�CaCO3�� CaCO3 + 2H+= Ca2++ H2O + CO2��
B. ���Ե缫��ⱥ��MgCl2��Һ�� Mg2++2Cl�� + 2H2O ![]() Mg(OH)2�� + H2�� + Cl2��
Mg(OH)2�� + H2�� + Cl2��
C. ��������Һ��ͨ��������CO2��![]() +H2O+CO2��
+H2O+CO2��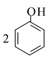 +
+![]()
D. ��������Һ������ȩ�е�ȩ����CH3CHO��![]() ��2OH��
��2OH��![]() CH3COONH4��H2O��2Ag����3NH3��
CH3COONH4��H2O��2Ag����3NH3��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com