
【题目】将4g NaOH溶解在10 mL水中,稀释至1 L后,再取出10 mL,这时的物质的量浓度为 ( )
A. 0.01 mol/LB. 0.1 mol/LC. 1 mol/LD. 无法精确
科目:高中化学 来源: 题型:
【题目】【2014全国大纲卷】
苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:

制备苯乙酸的装置示意图如下(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是 ;仪器c的名称是 ,其作用是 。
反应结束后加适量冷水,再分离出苯乙酸粗品。加人冷水的目的是 。下列仪器中可用于分离苯乙酸粗品的是 (填标号)。
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(3)提纯粗苯乙酸的方法是 ,最终得到44 g纯品,则苯乙酸的产率是 。
(4)用CuCl2 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是 。
(5)将苯乙酸加人到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一定量的铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+与 Fe3+的物质的量浓度之比为3∶2。则已反应的Fe3+与未反应的Fe3+的物质的量之比是( )
A. 1∶1 B. 1∶2 C. 2∶1 D. 2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素A、B、C、D、E、F、G在元素周期表中的位置如图1所示。

回答下列问题:
(1)G的基态原子核外电子排布式为___________;原子的第一电离能:D_____E(填“>”或“<”)。
(2)根据价层电子对斥理论,A2C中的“A—C—A”键角是_________(填字母序号)。
A.180° B.接近120°,但小于120°
C.接近120°,但大于120 D.接近109°28ˊ,但小于109°28ˊ
(3)已知化合物G(BC)5的G元素化合价为0,熔点为-20℃,沸点为103℃,其固体属于_______晶体,该物质中存在的化学键类型有________,它在空气中燃烧生成红棕色氧化物,反应的化学方程式为_________________________。
(4)化合物BCF2的分子立体构型为________,其中B原子的杂化轨道类型是_________。写出一个与BCF2具有相同空间构型的含氧酸根离子符号_____________。
(5)化合物EC的晶胞结构如图2所示。每个晶胞中含有_______个E2+。若EC晶体的密度为dg·cm-3,阿伏伽德罗常数值为NA,则晶胞参数a=_________nm(列出计算式,不要求最终结果)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数,下列说法正确的是( )
A.Na2O2与水反应时,1 mol Na2O2转移1 mol电子
B.78gNa2O2含有阴、阳离子总数是4NA
C.1mo1L﹣1的AlC13溶液中,C1﹣离子的数目为3 NA
D.5.6 g铁与足量盐酸反应转移的电子数为0.3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“HI(s)→HI(g)→H2和I2”的变化过程中,被破坏的作用力依次是( )
A. 范德华力、范德华力B. 共价键、离子键
C. 范德华力、共价键D. 共价键、共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源、环保等方面有着广泛的用途。实验室用氯化钠、废铁屑、稀硫酸、氢氧化钾溶液等为原料,通过以下过程制备高铁酸钾(K2FeO4):

(l) Na2O2的电子式为__________。
(2)操作I的步骤为蒸发浓缩、冷却结晶、过滤、洗涤、隔绝空气减压干燥.其中隔绝空气减压干燥的目的是_______。
(3)气体X为____,写出FeSO4与Na2O2反应的化学方程式:________。
(4)最终在溶液中可得到K2FeO4 晶体的原理是_________。
(5)已知K2FeO4在水溶液中可以发生:4FeO42-+10H2O![]() 4Fe(OH)3(胶体)+8OH-+3O2↑,,则K2FeO4 可以在水处理中的作用是__________。
4Fe(OH)3(胶体)+8OH-+3O2↑,,则K2FeO4 可以在水处理中的作用是__________。
(6)称取提纯后的K2FeO4样品0.2100g于烧杯中,加入强碱性亚铬酸盐溶液,反应后再加稀硫酸调节溶液呈强酸性,配成250mL 溶液,取出25.00 mL放入锥形瓶,用0.0l000mol/L的(NH4)2Fe(SO4)2溶液滴定至终点,重复操作2次,平均消耗(NH4)2Fe(SO4)2溶液30.00mL。涉及的主要反应为:Cr(OH)4-+FeO42-=Fe(OH)3+CrO42-+OH-
Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O
则该K2FeO4样品的纯度为______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4溶液,下列各图中表示其产生氢气总体积(V)与时间(t)的关系正确的是( )
A.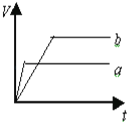 B.
B.
C. D.
D.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com