
【题目】有机物A有果香味,现用A合成聚酯L,过程如下图所示。
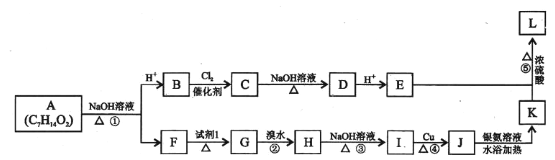
已知:(1)有机物B和F的相对分子质量相等,H有支链。
(2)已知:![]()
回答下列问题:
(I)试剂I的名称是____________________________。
(2)请用系统命名法给有机物H命名,其名称是_________________________。
(3) ①、②、③、④、⑤中属于取代反应的是___________________(填标号)。
(4)有机物F的结构简式可能是_______________________________。
(5) C生成D的化学方程式是______________________________。
(6) J生成K的化学方程式是______________________________。
(7)有机物E在浓硫酸的作用下,可生成一种6元环状化合物,该环状化合物的等效氢有_____种。
(8)有机物M是E的同系物,M的相对分子质量比E大14。满足下列条件的与M具有相同分子式的同分异构体共有_____种(不考虑立体异构)。
①能发生水解反应 ②能与金属钠反应 ③不含![]()
【答案】 浓硫酸 2-甲基-1,2-二溴丙烷 ①、③、⑤ (CH3)2C(OH)CH3、(CH3)2CHCH2OH CH3CHClCOOH+2NaOH![]() CH3CH(OH)COONa+NaCl+H2O (CH3)2C(OH)CHO+2Ag(NH3)2OH
CH3CH(OH)COONa+NaCl+H2O (CH3)2C(OH)CHO+2Ag(NH3)2OH![]() (CH3)2C(OH)COONH4+2Ag↓+3NH3+H2O 2 11
(CH3)2C(OH)COONH4+2Ag↓+3NH3+H2O 2 11
【解析】有机物A有果香味,且在氢氧化钠溶液中水解生成醇和羧酸钠,故A为饱和一元酯,根据A的化学式C7H14O2,以及已知:有机物B和F的相对分子质量相等,H有支链。推出醇F化学式为C4H9OH,且也有支链,应该为(CH3)2CHCH2OH,羧酸B为CH3CH2COOH,结合已知条件以及流程可推出:C为:CH3CHClCOOH,D为:CH3CH(OH)COONa,E为:CH3CH(OH)COOH,F到G引入碳碳双键,故试剂I为浓硫酸,发生消去反应生成的G为:(CH3)2CH=CH2,H为:(CH3)2CHBrCH2Br,I为:(CH3)2CH(OH)CH2OH,J为: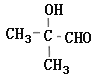 ,K为:
,K为: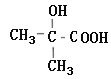 ;则
;则
(1)试剂I的名称是浓硫酸;(2) (CH3)2CHBrCH2Br系统命名是2-甲基-1,2-二溴丙烷;(3) ①、②、③、④、⑤中属于取代反应的是①、③、⑤,②为加成反应,④为氧化反应;(4)有机物F的结构简式是(CH3)2CHCH2OH;(5) C在氢氧化钠的水溶液中加热发生水解反应生成D的化学方程式是CH3CHClCOOH+2NaOH![]() CH3CH(OH)COONa+NaCl+H2O ;(6) J在银氨溶液中水浴加热发生银镜反应生成K的化学方程式是(CH3)2C(OH)CHO+2Ag(NH3)2OH
CH3CH(OH)COONa+NaCl+H2O ;(6) J在银氨溶液中水浴加热发生银镜反应生成K的化学方程式是(CH3)2C(OH)CHO+2Ag(NH3)2OH![]() (CH3)2C(OH)COONH4+2Ag↓+3NH3+H2O;(7)有机物E在浓硫酸的作用下,可生成一种6元环状化合物酯,该环状化合物的等效氢有2种;(8)相对分子质量比CH3CH(OH)COOH大14的同系物M,多一个CH2,M的同分异构体满足①能发生水解反应,则含有酯基, ②能与金属钠反应,除了酯基外,另一个氧应该是形成羟基, ③不含
(CH3)2C(OH)COONH4+2Ag↓+3NH3+H2O;(7)有机物E在浓硫酸的作用下,可生成一种6元环状化合物酯,该环状化合物的等效氢有2种;(8)相对分子质量比CH3CH(OH)COOH大14的同系物M,多一个CH2,M的同分异构体满足①能发生水解反应,则含有酯基, ②能与金属钠反应,除了酯基外,另一个氧应该是形成羟基, ③不含![]() 则可看成酯中一个氢被羟基取代,若为甲酸酯,有HCOOCH2CH2CH3和HCOOCH(CH3)2,HCOOCH2CH2CH3被羟基取代有3种;HCOOCH(CH3)2被羟基取代有2种;若为乙酸酯,有CH3COOCH2CH3,被羟基取代有3种;若为丙酸酯,有CH3CH2COOCH3,被羟基取代有3种;总共有11种同分异构体符合条件。
则可看成酯中一个氢被羟基取代,若为甲酸酯,有HCOOCH2CH2CH3和HCOOCH(CH3)2,HCOOCH2CH2CH3被羟基取代有3种;HCOOCH(CH3)2被羟基取代有2种;若为乙酸酯,有CH3COOCH2CH3,被羟基取代有3种;若为丙酸酯,有CH3CH2COOCH3,被羟基取代有3种;总共有11种同分异构体符合条件。


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
【题目】NH3可用于制氮肥![]() 尿素、碳铵等
尿素、碳铵等![]() 、HNO3、铵盐、纯碱,还可用于制合成纤维、塑料、染料等。回答下列问题:
、HNO3、铵盐、纯碱,还可用于制合成纤维、塑料、染料等。回答下列问题:
(1)传统的联氨(N2H4)合成方法是用NaClO溶液氧化NH3得到,反应的化学方程式为________________。联氨的电子式为________________。
(2)已知①N2(g)+3H2(g)2NH3(g) H=-92.4kJ/mol,②N2H4(l)+O2(g)N2(g)+2H2O(l) H=-624kJ/mol,则反应2NH3(g) +2H2O(l)N2H4(l)+O2(g) +3H2(g)的H=________,该反应的平衡常数表达式为________________,在常温下该反应________(填“能”或“不能”)自发进行。为了提高N2H4的产率,下列措施可行的是____________________。
A.增加H2O(l)的量B.增大压强C.降低温度 D.及时导出O2
(3)现在采用电解法合成氨,在电解法合成氨的过程中,用石墨作电极,阳极通入________________,阴极通入________________,阴极的电极反应式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质之间的化学反应,反应产物一定为纯净物的是
A.CH3CH3+Cl2![]()
B.CH3-CH=CH-CH3+Br2
C.CH2=CH-CH2-CH3+HCl![]()
D.CH3-CH=CH2+H2O![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在人类文明的历程中,改变世界的事物很多,其中铁、硝酸钾、青霉素、氨、乙醇、二氧化碳等17种“分子”改变过人类的世界。
(1)铁原子在基态时,价层电子排布式为___。
(2)硝酸钾中NO3-的空间构型为___。
(3)1molCO2分子中含有σ键的数目为___。乙醇的相对分子质量比氯乙烷小,但其沸点比氯乙烷高,其原因是___。
(4)6-氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有___。
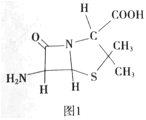
(5)铁和氨气在640℃可发生置换反应,产物之-的晶胞结构如图2所示,写出该反应的化学方程式___。
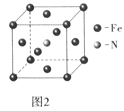
(6)晶胞有两个基本要素:
①原子坐标参数:表示晶胞内部各微粒的相对位置。如图是CaF2的晶胞,其中原子坐标参数A处为(0,0,0);B处为(![]() ,
,![]() ,0);C处为(1,1,1)。则D处微粒的坐标参数为___。
,0);C处为(1,1,1)。则D处微粒的坐标参数为___。
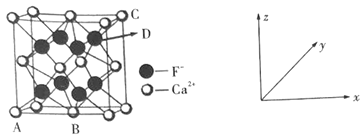
②晶胞参数:描述晶胞的大小和形状。已知CaF2晶体的密度为ρg·cm-3,则晶胞参数a为___pm(设NA为阿伏加德罗常数的值,用含ρ、NA的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学家运用穿山甲的鳞片特征,制作出具有自我恢复性的防弹衣,具有如此神奇功能的是聚对苯二甲酰对苯二胺(G)。其合成路线如下:
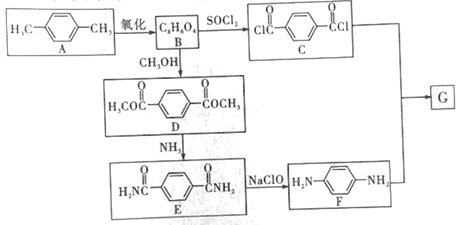
回答下列问题:
(1)A的化学名称为___。
(2)B中含有的官能团名称为___,B→C的反应类型为___。
(3)B→D的化学反应方程式为___。
(4)G的结构简式为___。
(5)芳香化合物H是B的同分异构体,符合下列条件的H的结构共有___种(不考虑立体异构),其中核磁共振氢谱有四组峰的结构简式为___。
①能与NaHCO3溶液反应产生CO2;②能发生银镜反应
(6)参照上述合成路线,设计以![]() 为原料(其他试剂任选),制备
为原料(其他试剂任选),制备![]() 的合成路线:___。
的合成路线:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A. 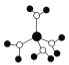 水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
B. 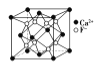 CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
C.  H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
D.  金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F(C21H20O6)在临床医学上具有预防肿瘤的作用,其合成路线如下,其中反应③中反应物的原子利用率为100%。
已知:Ⅰ. ![]()
![]()
![]() +H2O
+H2O
Ⅱ. ![]()
![]()
![]() +CO2
+CO2
Ⅲ. ![]() +
+![]()
![]()
![]() +H2O
+H2O
请回答下列问题:
(1) B中含有的官能团名称是____________。
(2)反应①的化学方程式是____________。 反应④的化学方程式是____________。
(3) F的结构简式是____________。
(4) E的同分异构体中,同时符合下列两个条件的共有__________种,其中核磁共振氢谱中有4组吸收峰的同分异构体的结构简式为__________。
①苯环上的一取代物只有2种;
②1mol该物质与足量NaOH溶液反应时,反应消耗3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.向蒸馏水中滴加浓H2SO4时,![]() 不变
不变
B.常温下,0.01mol·L-1Ba(OH)2溶液pH为12
C.常温下,CH3COOH稀溶液中加水稀释,则![]() 减小
减小
D.常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使溶液的pH减小且![]() 的值增大
的值增大
查看答案和解析>>
科目:高中化学 来源: 题型:
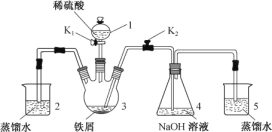
【题目】某同学设计如图装置(气密性已检查)制备Fe(OH)2白色沉淀。
请回答:
(1) 仪器1的名称________。装置5的作用________。
(2) 实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使溶液能进入4中________。
(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com