
【题目】氯苯是染料、医药、有机合成的中间体,是重要的有机化工产品。实验室制取氯苯的装置如图所示(加热和固定仪器的装置已略去)。
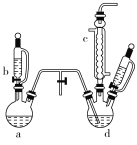
回答下列问题:
(1)如果用a和b仪器组合成制取氯气的装置,反应无需加热,则a仪器中的固体反应物可以是________(填序号)。
A.MnO2 B.KMnO4 C.K2Cr2O7
(2)仪器c的名称是________。
(3)制取氯苯的化学方程式为________________。
(4)仪器d中的反应完成后,工业上要进行水洗、碱洗及食盐干燥,才能蒸馏。碱洗之前要进行水洗,其目的是______________________。
(5)生成的氯气中存在HCl、H2O等杂质气体,若需要增加一个装置除去水蒸气,请在下框中画出,并标明所用试剂。
__________
(6)工业生产中苯的流失情况如表所示:
项目 | 二氯苯 | 氯化尾气 | 蒸气 | 成品 | 不确定苯耗 | 合计 |
苯流失量/(kg·t-1) | 11.7 | 5.4 | 20.8 | 2.0 | 49.3 | 89.2 |
则10 t苯可制得成品氯苯________t。(列出计算式即可。氯苯和苯的相对分子质量分别是112.5和78)
【答案】BC 球形冷凝管 ![]() +Cl2
+Cl2![]()
![]() +HCl 洗去FeCl3、HCl等无机物;节省碱的用量,降低成本
+HCl 洗去FeCl3、HCl等无机物;节省碱的用量,降低成本 
![]()
【解析】
(1)高锰酸钾和重铬酸钾制备氯气不用加热;
(2)根据仪器构造c为球形冷凝管;
(3)由苯和氯气在催化剂的条件下制取氯苯;
(4)d中反应完成后有FeCl3、HCl等副产品,易溶于水;
(5)可用浓硫酸吸收水蒸气;
(6)根据苯的总流失量计算参加反应的苯的质量,再根据苯与氯苯质量定比关系计算.
:(1)二氧化锰制氯气需要加热,高锰酸钾和重铬酸钾不用,故答案为:BC;
(2)仪器c为球形冷凝管;故答案为:(球形)冷凝管;
(3)制取氯苯的化学方程式为:. ![]() +Cl2
+Cl2![]()
![]() +HCl ;故答案为:.
+HCl ;故答案为:. ![]() +Cl2
+Cl2![]()
![]() +HCl ;
+HCl ;
(4)d中反应完成后有FeCl3、HCl等副产品,易溶于水,碱洗之前要水洗,可以洗去这些无机物,节约碱的用量,降低成本;故答案为:洗去FeCl3、HCl等无机物。节省碱的用量,降低成本;
(5)浓硫酸可用于吸收水蒸气,为充分吸收,导气管应长进短出,装置为: ;
;
(6)苯的总流失量为89.2kg/t,故1t苯中参加反应的苯的质量为(1t-0.0892t),由苯与氯苯质量之比为78:112.5,则10t苯可制得成品氯苯为:![]() t;故答案为:
t;故答案为:![]() 。
。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】对于2SO2(g)+O2(g) 2SO3(g),ΔH<0,根据下图,下列说法错误的是( )

A.t2时使用了催化剂B.t3时采取减小反应体系压强的措施
C.t5时采取升温的措施D.反应在t6时刻,SO3体积分数最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有结构简式如图所示的某有机物,它是药物生产的中间体,关于该有机物叙述正确的是
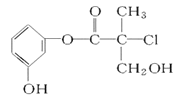
A.该有机物能与Na2CO3发生反应
B.该有机物与浓硫酸混合加热可发生消去反应
C.1mol该有机物与足量NaOH溶液反应最多消耗3molNaOH
D.该有机物经催化氧化后能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向0.1mol/I.的NH4HCO3溶液中逐渐加入0.1mol/LNaOH溶液时,含氮、含碳粒子的分布情况如图所示(纵坐标是各粒子的分布系数,即物质的量分数)。根据图象,下列说法不正确的是( )

A. 开始阶段,HCO3-反而略有增加,可能是因为NH4HCO3溶液中存在H2CO3发生的主要反应是H2CO3+OH-═HCO3-+H2O
B. 当pH大于8.7以后,碳酸氢根离子和铵根离子同时与氢氧根离子反应
C. pH=9.5时,溶液中c(HCO3-)>c(NH3H2O)>c(NH4+)>c(CO32-)
D. 滴加氢氧化钠溶液时,首先发生的反应为2NH4HCO3+2NaOH═(NH4)2CO3+Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)粗制CuSO4·5H2O晶体中常含有杂质Fe2+。
①在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质最好选用的是________。
A.KMnO4 B.H2O2 C.氯水 D.HNO3
②然后再加入适当物质调整溶液至pH=4,使Fe3+转化为Fe(OH)3,调整溶液pH可选用下列中的_______。
A.NaOH B.NH3·H2O C.CuO D.Cu(OH)2
(2)在25 ℃下,向浓度均为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式),生成该沉淀的离子方程式为________。已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
(3)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,![]() =____。已知Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10。
=____。已知Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作、现象和解释或结论都正确的( )
选项 | 实验操作 | 现象 | 解释或结论 |
① | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
② | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
③ | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
④ | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
⑤ | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
⑥ | 将H2O2溶液滴入KMnO4溶液中 | KMnO4溶液褪色 | 2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O |
⑦ | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
⑧ | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下反应 |
A.①④⑤⑥⑦B.④⑤⑥C.④⑤⑥⑦D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验。
[分子式的确定]
(1)将有机物A置于氧气流中充分燃烧,实验测得生成5.4 g H2O和8.8 g CO2,消耗氧气6.72 L(标准状况下)。则该物质中各元素的原子个数比是___。
(2)质谱仪测定有机化合物的相对分子质量为46,则该物质的分子式是____。
(3)根据价键理论,预测A的可能结构并写出结构简式____。
[结构式的确定]
(4)经测定,有机物A的核磁共振氢谱如图所示,则A的结构简式为___。
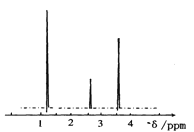
[性质实验]
(5)A在Cu作用下可被氧化生成B,其化学方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
2R—C≡C—H![]() R—C≡C—C≡C—R+H2
R—C≡C—C≡C—R+H2
该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的结构简式为______,D 的化学名称为______。
(2)①和③的反应类型分别为______、______。
(3)E的结构简式为______。用1 mol E合成1,4二苯基丁烷,理论上需要消耗氢气_______mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为_____________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中3种的结构简式_______________________________。
(6)写出用2苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家石油化工的发展水平,请回答下列问题。
(1)乙烯的电子式为________,结构简式为________。
(2)鉴别甲烷和乙烯的试剂可以是________(填序号)。
A.稀硫酸 B.溴水 C.水 D.酸性高锰酸钾溶液
(3)下列物质中,可以通过乙烯加成反应得到的是________(填序号)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(4)已知![]() 。若以乙烯为主要原料合成乙酸,其合成路线如图所示。
。若以乙烯为主要原料合成乙酸,其合成路线如图所示。
![]()
反应②的化学方程式为________________。
(5)工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物聚乙烯,其反应的化学方程式为________________,反应类型是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com