
| A. | 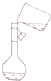 定容 | B. | 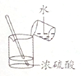 稀释浓硫酸 | C. | 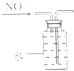 排水法收集NO | D. |  实验室制氨气 |
分析 A.配制一定物质的量浓度的溶液时,应该用胶头滴管定容;
B.稀释浓硫酸时,应该将浓硫酸倒入水中,顺序不能颠倒;
C.NO气体不溶于水,可用排水法收集;
D.氯化铵加热分解生成氯化氢和氨气,但是氨气与氯化氢在试管口附近又会反应生成氯化铵.
解答 解:A.定容时不能向容量瓶中直接用烧杯倒入蒸馏水,否则难以控制加入水的量,应该用胶头滴管定容,故A错误;
B.图示稀释方法容易导致液态四溅,应该将浓硫酸缓缓倒入水中,故B错误;
C.一氧化氮不溶于水,可通过排水法收集NO气体,图示装置合理,故C正确;
D.不能用加热氯化铵的方法制取氨气,实验室中通常用加热氢氧化钙、氯化铵固体制备氨气,图示原理不合理,故D错误;
故选C.
点评 本题考查了化学实验装置特点及判断,题目难度中等,明确化学实验基本操作方法为解答关键,注意掌握常见气体的性质及制取、收集方法,试题培养了学生的分析能力及化学实验能力.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:填空题
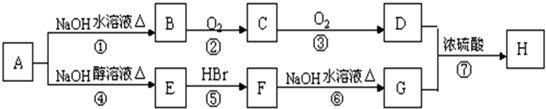
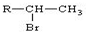 (R为烃基)
(R为烃基)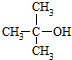 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
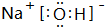 ,CB2的电子式为
,CB2的电子式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
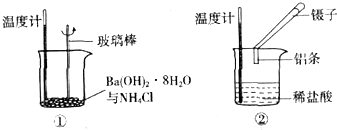
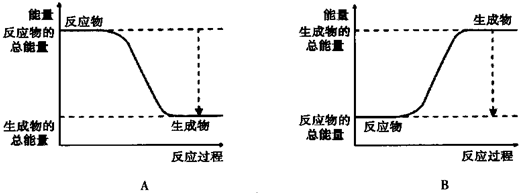
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验事实 | 结论 | |
| A | 加碱加热产生使湿润红色石蕊试纸变蓝的气体 | 溶液中含有NH4+ |
| B | 加BaCl2溶液有白色沉淀,加稀硝酸沉淀不溶解 | 该溶液中一定含有SO42- |
| C | 加KSCN溶液无现象•再滴加氯水变血红 | 溶液中有Fe2+ |
| D | 加热时.铜能与浓硫酸反应 | 浓硫酸有强氧化性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石硬度很高,用于制作精美首饰 | |
| B. | C60分子可镶入金属钾,用做高温超导体 | |
| C. | 石墨熔沸点高,用做飞船表面隔热材料 | |
| D. | 碳纳米管导电性好,用于制作大规模集成电路 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
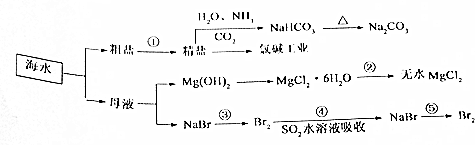
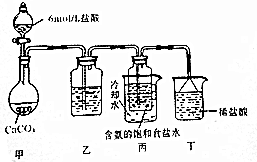
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升温 | B. | 加压 | C. | 减压 | D. | 降温 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com