
【题目】黑火药是我国的四大发明之一,深受世人称赞,其反应原理为:
S+3C+2KNO3![]() N2↑+3CO2↑+K2S
N2↑+3CO2↑+K2S
请回答下列相关问题:
(1)当产生0.1molN2时,反应中共转移电子数为_____,还原剂的物质的量为_____mol。
(2)若生成标准状况下33.6LCO2,则被S氧化的C的物质的量是_____mol。
【答案】 1.2×6.02×1023或7.224×1023或1.2NA 0.3 0.25
【解析】 (1). S + 3C + 2KNO3![]() N2↑+3CO2↑+K2S
N2↑+3CO2↑+K2S
↓2 ↑3![]() 4 ↓2
4 ↓2![]() 5
5
分析反应原理可知,反应中元素化合价升高的只有碳元素(从0升到+4),但降低的有硫(从0降到-2))和氮(从+5降到0)两种,碳是还原剂,硫和硝酸钾是氧化剂,每生成1molN2就一定有3molC失去12mole-被氧化,所以当有0.1molN2生成时,反应中转移电子数为1.2×6.02×1023或7.224×1023或1.2NA ,消耗还原剂C的物质的量为 0.3 mol.
(2). n(CO2)= ![]()
由上述分析可知,当有3molC被氧化时生成3molCO2,C共失去12mole-,S得到其中的2mol,占![]() ,说明有
,说明有![]() 的C被S氧化,所以当有1.5mol CO2生成时,被S氧化的C的物质的量为1.5
的C被S氧化,所以当有1.5mol CO2生成时,被S氧化的C的物质的量为1.5![]() =0.25mol.
=0.25mol.


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
【题目】在接触法制硫酸的生产中,SO2转化成SO3转化率的大小直接决定生产效率。某研究小组用下图装置模拟生产过程中测定SO2转化成SO3的转化率。已知SO3的熔点是16.8℃,沸点是44.8℃。装置Ⅰ中所涉及反应的化学方程式为: 。
(1)Ⅱ中的试剂是 ,仪器Ⅵ的名称为 。装置Ⅲ发生反应的化学方程式是 。
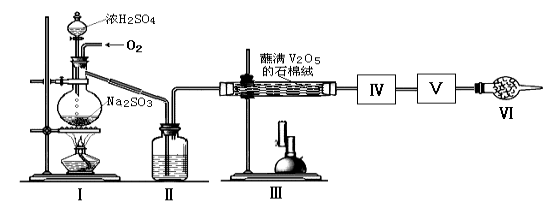
(2)根据实验需要,应该在Ⅳ、Ⅴ处连接合适的装置。请从下图A~D装置中选择最适合装置并将序号填入下面的空格中,Ⅳ、Ⅴ处连接的装置分别是 、 。
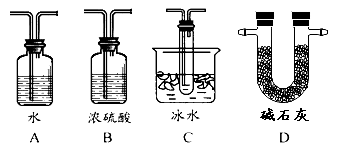
(3)为了提高SO2的转化率,实验时在:①滴加浓硫酸;②加热催化剂的步骤中,应采取的操作是先后顺序_____________(填编号)。
(4)实验结束后,如果把收集SO3的试管敞口露置于空气中,能够看到管口有大量的白雾,产生此现象的原因是 。
(5)用18.9gNa2SO3粉末与足量较浓的硫酸进行此实验,当反应结束时,继续通入O2一段时间后测得装置Ⅴ增重了7.2g,则实验测得SO2的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体的体积主要由以下什么因素决定的:①气体分子的直径 ②气体物质的量的多少 ③气体分子间的平均距离 ④气体分子的相对分子质量( )
A.①②
B.①③
C.②③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
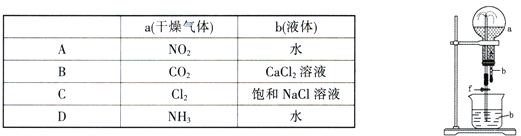
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学电源的叙述错误的是( )
A. 普通锌锰干电池中碳棒为正极
B. 铅蓄电池中覆盖着PbO2的电极板是负极板
C. 氢氧燃料电池的正极是通入氧气的那一极
D. 碱性锌锰干电池的比能量和储存时间比普通锌锰干电池高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化 都符合的示意图的反应是 ( )
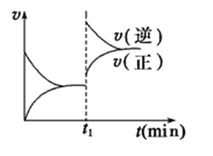
A. 2SO2(g)+O2(g)![]() 2SO3(g);△H<0
2SO3(g);△H<0
B. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g);△H<0
4NO(g)+6H2O(g);△H<0
C. H2(g)+I2(g)![]() 2HI(g);△H>0
2HI(g);△H>0
D. N2(g)+3H2(g)![]() 2NH3(g)△H<0
2NH3(g)△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是( )
A. ①②③④ B. ②③ C. ①②④ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器:①普通漏斗:②容量瓶:③蒸馏烧瓶:④天平;⑤分液漏斗:⑥滴定管:⑦燃烧匙。常用于物质分离的是
A. ①③④ B. ①②⑥ C. ①③⑤ D. ③④⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 通过石油分馏可以获得大量的芳香烃
B. 石油裂化的目的是为了得到乙烯、丙烯和苯
C. 煤的干馏发生了化学变化
D. 煤中含有苯和甲苯,可以通过先干馏后分馏的方法得到苯和甲苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com