
| A. | M极连接直流电源的正极 | |
| B. | 阳极上的电极反应为:NO-3e-+4OH-=NO3-+2H2O | |
| C. | 为使电解产物全部转化为NH4NO3浓溶液,需补充的物质X,则X为NH3 | |
| D. | 装置中加入稀NH4NO3溶液的目的是为了提高溶液的导电能力,可用NaNO3溶液代替 |
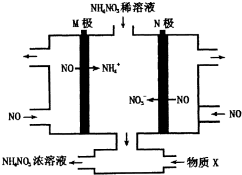
分析 电解NO制备NH4NO3,由图可知N为阳极反应为NO-3e-+2H2O=NO3-+4H+,M为阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总反应方程式为:8NO+7H2O$\frac{\underline{\;电解\;}}{\;}$3NH4NO3+2HNO3,因此若要使电解产物全部转化为NH4NO3,需补充NH3,据此分析.
解答 解:电解NO制备NH4NO3,由图可知N为阳极反应为NO-3e-+2H2O=NO3-+4H+,M为阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总反应方程式为:8NO+7H2O$\frac{\underline{\;电解\;}}{\;}$3NH4NO3+2HNO3,因此若要使电解产物全部转化为NH4NO3,需补充NH3;
A.根据以上分析,M电极为阴极,与电源的负极相连,故A错误;
B.由图可知N为阳极反应为NO-3e-+2H2O=NO3-+4H+,故B错误;
C.根据以上分析,则A为NH3,故C正确;
D.根据阳极反应为NO-3e-+2H2O=NO3-+4H+,阴极反应为:NO+5e-+6H+=NH4++H2O,当两极得失电子数目相等时,硝酸根根离子的浓度大于铵根,加入硝酸铵的目的为增强导电性,平衡电荷,钠离子不能代替铵根的作用,故D错误.
故选C.
点评 本题考查了电解原理的应用等,题目涉及的知识点较多,侧重于考查学生的综合运用能力,难度中等,注意基础知识的积累掌握.


科目:高中化学 来源: 题型:选择题
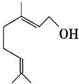 香叶醇是合成玫瑰香油的主要原料,结构可用键线式表示如图,键线式中每个端点和拐点处都代表有一个碳原子,氢原子可根据碳为四价的原则而相应地在碳上补充.下列有关香叶醇的叙述正确的是( )
香叶醇是合成玫瑰香油的主要原料,结构可用键线式表示如图,键线式中每个端点和拐点处都代表有一个碳原子,氢原子可根据碳为四价的原则而相应地在碳上补充.下列有关香叶醇的叙述正确的是( )| A. | 香叶醇的分子式为C10H18O | B. | 不能使溴的四氯化碳溶液褪色 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 能发生加成反应不能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 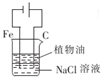 用图装置制取Fe(OH)2沉淀 | B. | 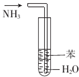 用图装置吸收NH3并防止倒吸 | ||
| C. | 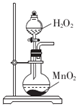 用图装置制取少量氧气 | D. | 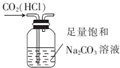 用图装置除去CO2中含有的少量HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

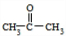 .
.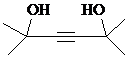 .
.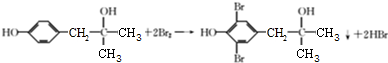 .
.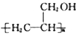 的合成路线图(无机试剂任用).合成路线图示例如下:
的合成路线图(无机试剂任用).合成路线图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
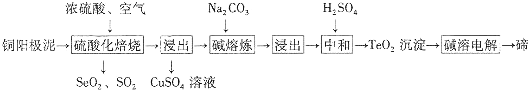
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 邻二甲苯只有一种结构,能证明苯环中不存在碳碳单键和碳碳双键交替的结构 | |
| B. | 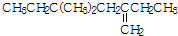 与氢气加成后的产物用系统命名法命名为3,5,5-三甲基庚烷 与氢气加成后的产物用系统命名法命名为3,5,5-三甲基庚烷 | |
| C. | 植物秸秆和土豆淀粉在一定条件下水解的产物都可以转化为酒精 | |
| D. | 完全燃烧一定质量的冰醋酸、葡萄糖混合物(以任意质量比混合),生成CO2和H2O的物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
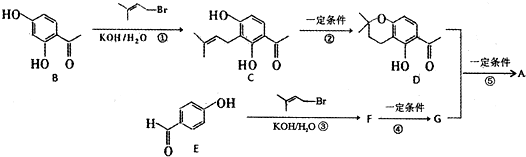
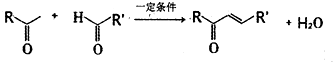
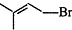 生成高分子化合物的方程式
生成高分子化合物的方程式 .
. 、
、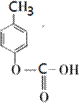 .
.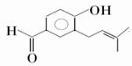 .
.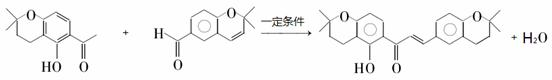 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
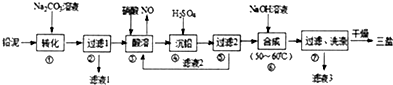
| A. | 步級①PbSO4转化为难溶PbCO3的离子方程式为CO32-+PbSO4=PbCO3+SO42- | |
| B. | 步骤③酸溶时,PbO、Pb、PbCO3都与硝酸反应生成Pb(NO3)2; 滤液2中可回收再利用的主要成分为HNO3 | |
| C. | 滤液1、滤液3中所含的溶质完全相同 | |
| D. | 步骤⑥合成三盐的化学方程式为4PbSO4+6NaOH=3Na2SO4+3PbO•PbSO4•H2O+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4与P4的分子结构都是正四面体形,因此在6.02×1023个CH4分子或P4分子中都含有4×6.02×1023个共价键 | |
| B. | 在含6.02×1023个硅原子的二氧化硅晶体中含有4×6.02×1023个Si-O键 | |
| C. | 28g CO、C2H4混合气体的分子总数NA,体积约为22.4L | |
| D. | 6.02×1023个Fe3+完全水解可以得到6.02×1023个氢氧化铁胶体粒子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com