
【题目】实验室制取乙炔的实验装置图(如图)中,
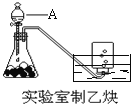
(1)A仪器的名称为_________________;所盛的试剂为_________________;发生反应的化学方程式为:__________________________________________________;
(2)将反应产生的乙炔通入酸性高锰酸钾溶液中,观察到的现象是:_________________;将反应产生的乙炔通入溴的四氯化碳溶液中,反应的化学方程式为:__________________________________;(产物为1,2-二溴乙烯)
(3)生成的乙炔中可能含有的杂质气体是_________________,除去的方法是_________________。
【答案】 分液漏斗 饱和食盐水 CaC2+2H2O→Ca(OH)2+CH≡CH↑ 酸性高锰酸钾溶液紫色褪去 ![]() 硫化氢、磷化氢(H2S、PH3) 将混合气体通过CuSO4溶液洗气
硫化氢、磷化氢(H2S、PH3) 将混合气体通过CuSO4溶液洗气
【解析】试题分析:实验室用电石和水反应制取乙炔,由于该反应十分剧烈,所以通常用饱和食盐水代替水并通过分液漏斗控制滴加的速度来减小反应速率。由于电石中常含有硫化钙和磷化钙等杂质,故所制备的乙炔中会混有硫化氢和磷化氢等杂质而有臭味。
(1)A仪器的名称为分液漏斗;所盛的试剂为饱和食盐水;发生反应的化学方程式为:CaC2+2H2O→Ca(OH)2+CH≡CH↑ ;
(2)将反应产生的乙炔通入酸性高锰酸钾溶液中,观察到的现象是酸性高锰酸钾溶液紫色褪去;将反应产生的乙炔通入溴的四氯化碳溶液中,生成1,2-二溴乙烯的化学方程式为![]() ;
;
(3)生成的乙炔中可能含有的杂质气体是硫化氢、磷化氢(H2S、PH3),除去的方法是将混合气体通过CuSO4溶液洗气。


科目:高中化学 来源: 题型:
【题目】绿色化学的目标是( )
A. 减少对环境的污染 B. 设计对人类健康和环境更安全的化合物
C. 防患于未然,最终杜绝化学污染源 D. 研究变换基本原料和起始化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的前三周期及其中的部分元素,请回答相关问题
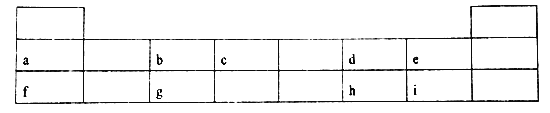
(1) a、f、g 元素最高价氧化物的水化物碱性由强到弱的顺序是__________(用化学式表示)。表中所给元素中金属性最强的与非金属性最强的形成的化合物溶液显______(填“中性“酸性”或“碱性” )。
(2) 氢元素可与其它元素形成_________(填选项序号)等化学键。
A.极性共价键 B.非极性共价键 C.氢键 D.离子键
(3)d、f、h三种元素可形成一种有强还原性的化合物,该化合物中含有非极性键,其化学式为____,向该化合物的水溶液中加入盐酸发生反应的离子方程式为______________。
(4)表中所给的某两种元素可形成一种常见的有机溶剂,可用于萃取碘水中的碘单质,萃取后有机层的颜色为___________,分液时有机层应从________(填“下口流出“或“上口倒出”)。该有机溶剂的电子式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】静脉注射时常用生理盐水(0.9%的氯化钠溶液)作为载体,将各种药物输入人体,该过程中生理盐水的功能主要是( )
A. 运输药物进入细胞 B. 提供能量
C. 维持细胞外液的渗透压 D. 供应水分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或对实验事实的叙述正确的是
①用稀盐酸洗涤盛放过石灰水的试剂瓶;
②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌;
③有六种分别含Na+、Mg2+、Al3+、Fe2+、Fe3+、NH4+阳离子的溶液,不能用NaOH溶液鉴别;
④用稀硝酸清洗做过银镜反应实验的试管;
⑤如果皮肤上不慎沾有苯酚,应立即用大量的NaOH稀溶液冲洗;
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
⑧向某溶液加入NaOH浓溶液并加热能产生能使湿润的红色石蕊试纸变蓝的气体则原溶液中含NH4+
A. ①⑤⑦ B. ③④⑦⑧ C. ①②④⑧ D. ②③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com