
【题目】对于下列反应:2SO2+O2![]() 2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为 ,用O2浓度变化来表示的反应速率为 .如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(Lmin),那么2min时SO2的浓度为 .
2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为 ,用O2浓度变化来表示的反应速率为 .如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(Lmin),那么2min时SO2的浓度为 .
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 通过石油分馏可以获得大量的芳香烃
B. 石油裂化的目的是为了得到乙烯、丙烯和苯
C. 煤的干馏发生了化学变化
D. 煤中含有苯和甲苯,可以通过先干馏后分馏的方法得到苯和甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2升的密闭容器中,发生以下反应: 2A(g)+ B(g) ![]() 2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是 ( )
2C(g)+D(g) 。若最初加入的A和B都是4 mol,在前10秒钟A的平均反应速度为0.12 mol/(L·s),则10秒钟时,容器中B的物质的量是 ( )
A.1.6 mol B.2.8 mol C.2.4 mol D.1.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的组成、分类和变化的说法正确的是
A. CO2、NO2、SO2均属于空气污染物
B. SiO2、CO、Al2O3均属于酸性氧化物
C. 胆矾、冰水混合物、双氧水都是混合物
D. 煤的干馏、气化和液化都是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对Al、Fe二种金属元素,下列说法正确的是
A. 铝能够稳定存在于空气中,而铁很容易生锈,说明铁比铝活泼
B. 等物质的量的Al、Fe分别与足量盐酸反应放出等质量的H2
C. 二者的氢氧化物都不可以通过氧化物化合反应直接制备
D. 二者的单质都能与强碱溶液反应生成H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒沙特列原理解释的是 ( )
A.用排饱和食盐水的方法收集氯气
B.在沸腾的蒸馏水中滴加FeCl3溶液,制Fe(OH)3胶体
C.在FeCl3溶液中加AgNO3溶液,产生白色沉淀
D.向AgCl 和水的悬浊液中加入足量的Na2S溶液并振荡,白色固体转化为黑色固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图曲线a表示放热反应( )
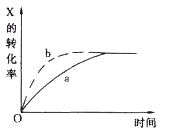
X(g)+Y(g)![]() Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
A.升高温度 B.加大X的投入量 C.加催化剂 D.增大体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 电子层结构相同的微粒,其化学性质—定相似
B. 第三周期非金属元素含氧酸的酸性从左到右依次增强
C. 非金属元素的原子两两结合形成的化合物不一定是共价化合物
D. 元素周期律是元素原子核外电子排布周期性变化的结果
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
(1)氧化产物是__________,还原产物是________。
(2)氧化剂与还原剂的物质的量之比是________。
(3)当有2 mol HNO3参加反应时,被氧化的物质是_____________ mol ,电子转移数目约为________个。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com