
【题目】下列关于原电池的叙述中正确的是( )
A.正极和负极必须是金属
B.原电池是把化学能转化成电能的装置
C.原电池工作时,正极和负极上发生的都是氧化还原反应
D.锌、铜和盐酸构成的原电池工作时,锌片上有6.5 g锌溶解,正极上就有0.1 g氢气生成
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下表为元素周期表中的一部分,列出了10种元素在元素周期表中的位置。试用元素符号、离子符号或化学式回答下列问题。
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
第2周期 | ⑥ | ⑦ | ||||||
第3周期 | ① | ③ | ⑤ | ⑧ | ⑨ | ⑩ | ||
第4周期 | ② | ④ |
(1)10
(2)①③⑤三种元素最高价氧化物对应水化物中,碱性最强的是 ,(填化学式)该物质内部含有的化学键类型是 和 ;
(3)元素⑦的氢化物的化学式为 ;该氢化物常温下和元素②的单质反应的化学方程式 ;
(4)③和⑨两元素形成化合物的电子式是 ;①和⑦两元素形成四核化合物的电子式是 ,该物质与CO2反应的化学方程式为 。
(5)①和⑤最高价氧化物对应水化物相互反应的离子方程式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
A. 950 mL, 111.2 g B. 500 mL, 117 g
C. 1000 mL, 117 g D. 1000 mL, 111.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中,不符合生产实际的是( )
A.电解熔融的氧化铝制取金属铝,用铁作阳极
B.电解法精炼粗铜,用纯铜作阴极
C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D.在镀件上电镀锌,用锌作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表各组物质之间通过一步反应就能实现如图所示转化的是
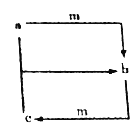
a | b | c | m | |
A | N2 | NO | HNO3 | O2 |
B | Na2CO3 | NaHCO3 | NaOH | CO2 |
C | H2S | S | SO2 | O2 |
D | CH3CH2OH | CH3CHO | CH3COOH | O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是( )
A. 含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 molL﹣1
B. 100 g硫酸溶液的物质的量浓度为18.4 molL﹣1,用水稀释到物质的量浓度为9.2 molL﹣1,需要水100 g
C. 配制一定物质的量浓度的氯化钾溶液:准确称取一定质量的氯化钾固体,放入到1000 mL的容量瓶中,加水1000 mL溶解,振荡摇匀
D. 将10 g CuSO4溶解在90 g水中,配制质量分数为10%的CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验误差分析中,不正确的是( )
A.用湿润的pH试纸测稀碱液的pH,测定值偏小
B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D.测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知N2O4和NO2可以相互转化:2NO2(g) ![]() N2O4(g) △H<0现将一定量N2O4和NO2的混合气体通入体积为2L的恒温密闭玻璃容器中,发生反应,各物质浓度随时间变化关系如图:
N2O4(g) △H<0现将一定量N2O4和NO2的混合气体通入体积为2L的恒温密闭玻璃容器中,发生反应,各物质浓度随时间变化关系如图:
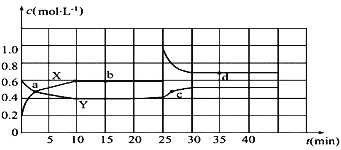
(1)图中曲线______(填“X”或“Y”)表示c(N2O4)随时间的变化。
(2)从起点开始首次达到平衡时,以NO2表示的反应速率为______。
(3)图中b点的平衡常数K的值为________。
(4)其他条件不变,若起始时向该容器中通入0.4molN2O4和0.2molNO2,则v正_____v逆(填“>”、“=”或“<”);若升温该反应的平衡常数K______(填“增大”、“减小”或“不变”) ,判断理由是_________________。
(5)25min时,改变的外界条件是______,图象中a、b、c、d四点中v正=v逆的点是____,四点中________点体系颜色最深。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,对于反应:CaCO3(块状)+2HCl===CaCl2+CO2↑+H2O,为加快反应速率,下列方法可行的有( )
①增加盐酸的浓度 ②增加同浓度盐酸的用量 ③加水 ④增加CaCO3(块状)的用量 ⑤将块状CaCO3改为粉末状CaCO3
A.1项 B.2项 C.3项 D.4项
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com