
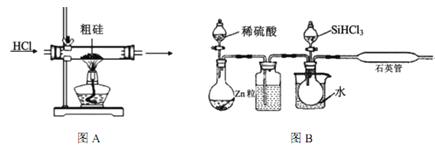
【题目】半导体工业需要高纯硅,粗硅中含有SiO2、Fe2O3、CuO、C等杂质,提纯硅的方法比较多,其中三氯氢硅(有一定毒性)氢还原法和四氯化硅氢还原法应用较为广泛,下面是实验室模拟工业上三氯氢硅氢还原法的基本原理:
已知:①Si+3HCl ![]() SiHCl3+H2(主要反应)
SiHCl3+H2(主要反应)
Si+4HCl![]() SiCl4+2H2(次要反应)
SiCl4+2H2(次要反应)
2NaCl+H2SO4(浓)![]() Na2SO4+2HCl↑
Na2SO4+2HCl↑
②典型硅的重要化合物的部分性质如下表:
熔点(℃) | 沸点(℃) | 溶解性 | |
SiHCl3 | -127 | 33 | 易溶于多数有机溶剂 |
SiCl4 | -23 | 77 | 易溶于多数有机溶剂 |
(1)粗硅在提纯前,需要进行酸、碱预处理,其目的是___________________________________。
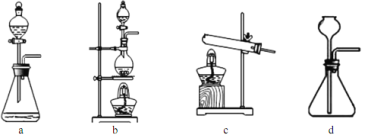
(2)下列装置在实验室可用于制备HCl气体的是_____(填字母代号)。
(3)在1100~1200℃条件下,利用图B在石英管中可以获得硅,写出该反应的方程式_______;其烧杯中水的作用是__________________________;该装置使用石英管而不是普通玻璃管的原因是_________。
(4)三氯氢硅氢还原法用 SiHCl3在图B中制硅,不足之处有_______________(任意回答一点即可)。
(5)SiCl4与氢气反应也能得到硅,但反应所需温度不同,在工业上往往将三氯氢硅中混入的SiCl4分离后再与氢气反应,你认为最好的分离方法是______________。
(6)工业上如果用四氯化硅氢还原法制硅,其原理如下:![]() 该方法与用三氯氢硅氢还原法比较,其缺点至少有两处,分别是_________________。
该方法与用三氯氢硅氢还原法比较,其缺点至少有两处,分别是_________________。
【答案】除去粗硅中SiO2、 Fe2O3、 CuO等杂质 a、b SiHCl3+H2 ![]() Si+3HCl 加热SiHCl3,以便使之变成蒸汽进入石英管 反应温度较高,普通玻璃不能承受该高温 没有进行尾气处理 蒸馏 使用了有毒气体;三氯氢硅氢还原法中HCl和H2可以直接循环利用,节约了成本,而四氯化硅氢还原法中没有可循环利用的原料
Si+3HCl 加热SiHCl3,以便使之变成蒸汽进入石英管 反应温度较高,普通玻璃不能承受该高温 没有进行尾气处理 蒸馏 使用了有毒气体;三氯氢硅氢还原法中HCl和H2可以直接循环利用,节约了成本,而四氯化硅氢还原法中没有可循环利用的原料
【解析】
通过粗硅中杂质的组成和性质,分析除杂的方法,根据题干信息选择正确的分离方法和实验装置。
(1)根据题干得粗硅中含有杂质,Fe2O3、 CuO能与酸反应,SiO2能与碱反应,故答案为:除去粗硅中SiO2、 Fe2O3、 CuO等杂质;
(2)由题干得,实验室中制备 HCl 气体是用固体NaCl和液体(浓硫酸)加热的反应,可选用装置b,实验室制备HCl也可采用向浓盐酸中滴加浓硫酸,则选用装置a,故可选用的装置为:a、b;
(3)由图示得反应的方程式为: SiHCl3+H2 ![]() Si+3HCl; 其烧杯中水的作用是:加热SiHCl3,以便使之变成蒸汽进入石英管; 该装置使用石英管而不是普通玻璃管的原因是:反应温度较高,普通玻璃不能承受该高温;
Si+3HCl; 其烧杯中水的作用是:加热SiHCl3,以便使之变成蒸汽进入石英管; 该装置使用石英管而不是普通玻璃管的原因是:反应温度较高,普通玻璃不能承受该高温;
(4) 由题干信息知三氯氢硅有毒,该装置不足之处在于:没有进行尾气处理;
(5)根据题干信息三氯氢硅和SiCl4沸点相差较大,最好的分离方法是蒸馏;
(6)由上述分析及题干信息知该方案的不足之处在于:使用了有毒气体;三氯氢硅氢还原法中HCl和H2可以直接循环利用,节约了成本,而四氯化硅氢还原法中没有可循环利用的原料。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
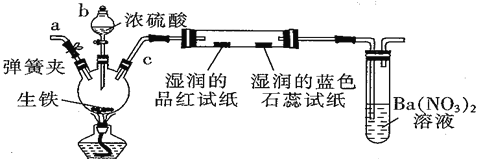
【题目】某化学兴趣小组为研究生铁(含少量碳)与浓硫酸的反应情况及产物性质,设计如下实验装置(夹持装置及尾气处理装置未画出)。请回答下列问题:
A B C
(1)仪器b 的名称为____________,按照上图装置进行实验,实验过程中,装置B中的现象是湿润的品红试纸__________________,湿润的蓝色石蕊试纸____________ 。若观察到装置C中会出现白色沉淀,原因是_____________________________。
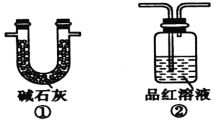

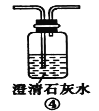
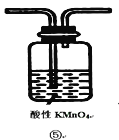
(2)装置A中还会产生能够使得澄清石灰水变浑浊的另一种气体,请写出产生该气体的化学方程式____________________________为了验证该气体,应从下列①~⑤中选出必要的装置连接装置A中出口C处,从左到右的顺序是_____________(填序号),连接好装置,然后打开弹簧夹a,多次鼓入N2,其目的是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的酸性强弱比较正确的是( )
A. HBrO4<HIO4 B. H2SO4<H3PO4 C. HClO3<HClO D. H2SO4>H2SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银的冶炼有很多方法, 在《 天工开物》 均有记载, 而现代流行的“ 氰化法”, 用 NaCN溶液浸出矿石中的银的方法是最常用的方法。 该方法具备诸多优点: 银的回收率高; 对游离态和化合态的银均能浸出; 对能源消耗相对较少; 生产工艺简便等, 但氰化物通常有毒。 其炼制工艺简介如下:

(1)矿石需要先进行破碎、 研磨, 其目的是__________。
(2)写出该工艺的一个明显的缺点__________ 。
(3)用 NaCN 浸泡矿石( 该矿石是辉银矿, 其主要成分是 Ag2S) 时, 反应容器处于开口状态, 产生的银以[Ag(CN)2]- 形式存在, 硫元素被氧化至最高价, 试写出主要反应的离子方程式__________。
(4)银往往和锌、 铜、 金等矿伴生, 故氰化法得到的银中往往因含有上述金属而不纯净, 需要进一步纯化, 从而获得纯净的银。 其中方法之一就是进行电解精炼, 在精炼过程中, 含有杂质的银作__________极( 填“阴” 或“阳”), 该电极上发生的主要反应式为__________, 金以__________形式存在。
(5)有人提出了另外的提纯银的方案, 先将锌粉还原后的混合金属用略过量的硝酸溶解, 通过精确调整溶液的 pH 来进行金属元素分离, 已知:
①溶解后的离子浓度如下表:
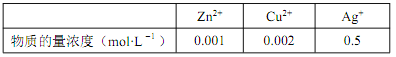
②某些金属离子的氢氧化物 Ksp如下:
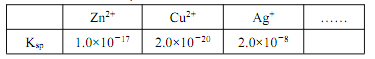
( 已知 lg2=0.3),该设计方案_______(填“ 可行” 或“ 不可行”),其原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素.
(1)该反应的离子方程式为 __________________________________ .
实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01molL-1、0.001molL-1,每次实验KMnO4酸性溶液的用量均为4mL、H2C2O4溶液(0.1molL-1)的用量均为2mL.在其它条件相同的情况下,某同学改变KMnO4酸性溶液的浓度,测得以下实验数据(从混合振荡均匀开始计时):
KMnO4酸性溶液的浓度/molL-1 | 溶液褪色所需时间t/min | ||
第1次 | 第2次 | 第3次 | |
0.01 | 14 | 13 | 11 |
0.001 | 6 | 7 | 7 |
(2)计算用0.001molL-1KMnO4酸性溶液进行实验时KMnO4的平均反应速率___________________________ (忽略混合前后溶液的体积变化).
(3)若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行? _____________________ .(填“行”或“不行”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在373 K时,密闭容器中充入一定量的NO2和SO2,发生如下反应:NO2(g)+SO2(g)![]() NO(g)+ SO3(g),平衡时,下列叙述正确的是
NO(g)+ SO3(g),平衡时,下列叙述正确的是
①NO和SO3的物质的量一定相等
②NO2和SO2的物质的量一定相等
③体系中的总物质的量一定等于反应开始时总物质的量
④SO2、NO2、NO、SO3的物质的量一定相等
A. ①和②B. ②和③C. ①和③D. ③和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组混合液:①四氯化碳和氯化钠溶液;②实验室制蒸馏水;③溴化钠和单质溴的水溶液.分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏B.萃取、蒸馏、分液C.分液、蒸馏、萃取D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学——选修3:物质的结构与性质)
钛有“生物金属”和“未来金属”之称,钛及其化合物的应用正越来越受到人们的关注。
(1)基态钛原子外围电子的轨道表达式为___________。与钛同周期的元素中,基态原子的未成对电子数与钛相同的有___种。
(2)金属钛的熔点、硬度均比铝大,可能的原因是____。
(3)TiCl4是氯化法制取钛的中间产物。TiCl4和SiCl4在常温下都是液体,分子结构相同。采用蒸馏的方法分离TiCl4和SiCl4的混合物,先获得的馏分是__________ (填化学式)。

(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯等的聚合,其结构如图所示。
①组成该物质的元素中,电负性最大的是__________ (填元素名称)。
②M中碳原子的杂化形式有___________种。
③M中不含__________ (填字母代号)。
a.π键 b.σ键 c.配位键
d.氢键 e.离子键

(5)①金属钛晶体中原子采用面心立方最密堆积,则晶胞中钛原子的配位数为_____。
②设钛原子的直径为d cm,用NA表示阿伏加德罗常数的值,钛原子的摩尔质量为M g·mol-1,则晶体钛的密度为________g·cm-3。
③金属钛晶胞中有若干个正四面体空隙,如图中a、b、c、d四个钛原子形成一个正四面体,其内部为正四面体空隙,可以填充其他原子。若晶胞中所有的正四面体空隙中都填充氢原子,那么形成的氢化钛的化学式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com