
设 NA为阿伏加德罗常数,下列有关叙述正确的是
A.78g过氧化钠晶体中,含NA个阴离子
B.56gFe 与稀 HN03 完全反应时一定转移3NA个电子
C.常温常压下,22.4L氦气含有NA个氦原子
D.已知热化学方程式2SO2(g)+O2(g) 2SO3(g)△H=-Q kJ?mol-1 (Q>0),则将 2NA 个SO2分子和 NA 个O2分子置于一密闭容器中充分反应后放出QkJ的热量
2SO3(g)△H=-Q kJ?mol-1 (Q>0),则将 2NA 个SO2分子和 NA 个O2分子置于一密闭容器中充分反应后放出QkJ的热量
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源:2015届福建省高三上学期第一次阶段考试化学试卷(解析版) 题型:选择题
下列有关实验的叙述正确的是( )
A.将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液
B.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH
C.用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应
D.读取滴定管内液体的体积,俯视读数导致读数偏小
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中质量检测化学试卷(解析版) 题型:填空题
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
| IA |
| 0 | |||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
|
2 |
|
|
| ② | ③ | ④ |
|
|
3 | ⑤ |
| ⑥ | ⑦ |
|
| ⑧ |
|
(1)④、⑤、⑥的离子半径由大到小的顺序是 (写离子符号)。
(2)③、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是________________(写化学式)。
(3)④、⑤中的某些元素可形成既含离子键又含共价键的化合物,写出其电子式:_____________。
(4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

则X溶液与Y溶液反应的离子方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中质量检测化学试卷(解析版) 题型:选择题
下列说法正确的是
A.HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高
B.熔融状态下能导电的化合物一定含离子键;金属与非金属元素形成的化合物一定是离子化合物
C.NaHSO4晶体中阴、阳离子的个数是1:2且熔化时破坏的是离子键和共价键
D.NCl3分子中所有的原子均为8电子稳定结构
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中质量检测化学试卷(解析版) 题型:选择题
不需要化学方法就能从人类的重要资源——海水中获得的物质是
A.食盐、淡水 B.钠、镁 C.氯气、烧碱 D.溴、碘
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期半期考试化学试卷(解析版) 题型:选择题
中学化学教材中,常借助于图像的这一表现手段清晰地突出实验装置的要点、形象地阐述化学过程的原理。下列有关化学图像表现的内容正确的是
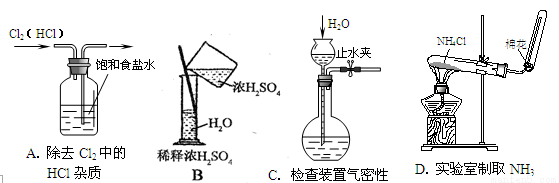
查看答案和解析>>
科目:高中化学 来源:2015届福建省四地六校高三上学期第一次月考化学试卷(解析版) 题型:填空题
(13分)已知工业盐中含有NaNO2,外观和食盐相似,有咸味,人若误食会引起中毒,致死量为0.3~0.5g。已知NaNO2能发生如下反应(方程式已配平):2NO2-+xI-+yH+=2NO↑+I2+zH2O,请回答下列问题:
(1)上述反应中,x =________, y =________,z =________,氧化剂是________________。
(2)根据上述反应,鉴别NaNO2和NaCl可选用的物质有:①碘化钾淀粉试纸、②淀粉、③食醋、④白酒,你认为必须选用的物质有________________(填序号)。
(3)某工厂废切削液中含有2%~5%的NaNO2,直接排放会造成水污染,但加入下列物质中的某一种就能使NaNO2转化为不引起污染的N2,该物质是________________。
A.NaCl B.KMnO4 C.浓硫酸 D.NH4Cl
(4)饮用水中的NO3- 对人类健康会产生危害,为了降低饮用水中NO3- 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3- 还原为N2,请配平化学方程式:
10Al+6NaNO3 + 4NaOH + 18H2O=□ ________ + 3N2↑。若反应过程中转移0.5mol电子,则生成标况下的N2体积为________。
查看答案和解析>>
科目:高中化学 来源:2015届福建省高二上学期半期联考化学试卷(解析版) 题型:选择题
(17分)电化学原理在日常生活和工农业生产中发挥着重要作用。钢铁生锈现象随处可见,钢铁的电化腐蚀原理如图所示:

(1)写出石墨电极的电极反应_________________________;
(2)将该装置作简单修改即可成为钢铁电化学防护的装置,请在上图虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向且完成以下问题
①简单修改后的该防护装置的名称为__________________________________
写出修改后石墨电极的电极反应式____________________________________;
②_______极(填“正极”“负极”“阳极”“阴极”)附近溶液的pH增大;
③检验阳极产物的方法是_____________________________________________;
④修改后的装置共收集到标准状况下的气体11.2 L时,则有______mol电子发生转移,假设溶液的体积为200ml,则此时溶液中OH-的物质的量浓度为________ mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com