
【题目】有机物X可通过如下方法合成。
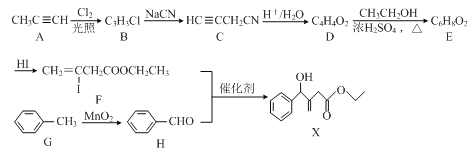
(1)G→H的反应类型为____反应。
(2)B的结构简式为____,E的结构简式为____。
(3)M与E互为同分异构体,且具有完全相同的官能团。M能发生银镜反应,核磁共振氢谱显示三种不同化学环境的氢,其峰面积之比为6∶1∶1。写出一种符合上述条件的M的结构简式____。
(4)请写出以CH3C≡CH、CH3OH为原料制取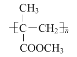 的合成路线示意图(无机试剂任用。合成示例例见本题题干)____。
的合成路线示意图(无机试剂任用。合成示例例见本题题干)____。
【答案】氧化 HC≡CCH2Cl HC≡CCH2COOCH2CH3 HCOOC≡CCH(CH3)2 ![]()
【解析】
(1)有机反应中加氧去氢的反应称之为氧化反应;
(2)A与氯气在光照条件下发生取代反应生成B,B与NaCN反应生成C,由A、C的结构简式知B的结构简式为HC≡CCH2Cl;C在H+/H2O条件下反应生成D,已知D的分子式为C4H4O2,且D与乙醇在浓硫酸加热的条件下反应,应为酯化反应,D的结构简式为HC≡CCH2COOH,E的结构简式为HC≡CCH2COOCH2CH3;
(3)E的分子式为C6H8O2,M与E互为同分异构体,且具有完全相同的官能团,则M的不饱和度为3,含有碳碳三键,酯基,M能发生银镜反应,则M应为甲酸某酯,核磁共振氢谱显示三种不同化学环境的氢,其峰面积之比为6∶1∶1,则含有三种等效氢,且个数比6:1:1;
(4)结合已知反应以及所学反应类型进行书写。
(1)有机反应中加氧去氢的反应称之为氧化反应,则G→H的反应类型为氧化反应;
故答案为:氧化;
(2)A与氯气在光照条件下发生取代反应生成B,B与NaCN反应生成C,由A、C的结构简式知B的结构简式为HC≡CCH2Cl;C在H+/H2O条件下反应生成D,已知D的分子式为C4H4O2,且D与乙醇在浓硫酸加热的条件下反应,应为酯化反应,D的结构简式为HC≡CCH2COOH,E的结构简式为 HC≡CCH2COOCH2CH3;
故答案为:HC≡CCH2Cl;HC≡CCH2COOCH2CH3;
(3)E的分子式为C6H8O2,M与E互为同分异构体,且具有完全相同的官能团,则M的不饱和度为3,含有碳碳三键,酯基,M能发生银镜反应,则M应为甲酸某酯,核磁共振氢谱显示三种不同化学环境的氢,其峰面积之比为6∶1∶1,则含有三种等效氢,且个数比6:1:1,符合上述条件的M的结构简式为:HCOOC≡CCH(CH3)2;
故答案为:HCOOC≡CCH(CH3)2;
(4)以CH3C≡CH、CH3OH为原料制取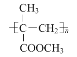 ,由该高分子的结构可知,其可由CH3C(COOCH3)=CH2通过加聚反应合成;而CH3C(COOCH3)=CH2可以由CH3C(COOH)=CH2与CH3OH通过酯化反应合成;由题干中C→D的信息可知,CH3C(COOH)=CH2可以由CH3C(CN)=CH2在酸性条件下水解生成;再由B→C的信息可知CH3C(CN)=CH2可以由CH3CBr=CH2与NaCN通过取代反应合成,而CH3CBr=CH2可由CH3C≡CH与HBr通过加成反应合成。具体合成路线示意图如下:
,由该高分子的结构可知,其可由CH3C(COOCH3)=CH2通过加聚反应合成;而CH3C(COOCH3)=CH2可以由CH3C(COOH)=CH2与CH3OH通过酯化反应合成;由题干中C→D的信息可知,CH3C(COOH)=CH2可以由CH3C(CN)=CH2在酸性条件下水解生成;再由B→C的信息可知CH3C(CN)=CH2可以由CH3CBr=CH2与NaCN通过取代反应合成,而CH3CBr=CH2可由CH3C≡CH与HBr通过加成反应合成。具体合成路线示意图如下:![]() ;
;
故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】对于可逆反应mA(s)+nB(g)![]() eC(g)+fD(g),当其他条件不变时,C的体积分数[φ(C)]在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是( )
eC(g)+fD(g),当其他条件不变时,C的体积分数[φ(C)]在不同温度(T)和不同压强(p)下随时间(t)的变化关系如图所示。下列叙述正确的是( )
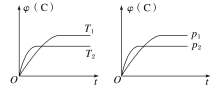
A.达到平衡后,若使用催化剂,C的体积分数将增大
B.该反应的ΔH<0
C.化学方程式中,n>e+f
D.达到平衡后,增加A的质量有利于化学平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于反应CH3COOH(l) + C2H5OH(l) ![]() CH3COOC2H5(l) + H2O(l) ΔH=-2.7kJ·mol-1,下列说法正确的是
CH3COOC2H5(l) + H2O(l) ΔH=-2.7kJ·mol-1,下列说法正确的是
A.由于水为液态,移走生成的水平衡不会移动。
B.因为化学方程式前后物质的化学计量数之和相等,所以反应的ΔS等于零
C.因为反应的△H 接近于零,所以温度变化对平衡转化率的影响大
D.因为反应前后都是液态物质,所以压强变化对化学平衡的影响可忽略不计
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨的催化氧化是工业制硝酸的重要反应:4NH3+5O2![]() 4NO+6H2O,对于该反应判断正确的是
4NO+6H2O,对于该反应判断正确的是
A. 氧气被还原B. 该反应是置换反应
C. 氨气是氧化剂D. 若有17 g氨参加反应,反应中转移10 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合氯气的相关知识解决下列问题。
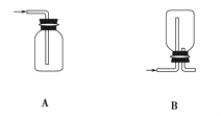
(1)在实验室中制取Cl2,下列收集Cl2的装置中正确的是_______(填字母)。

漂白粉能与盐酸发生反应,但盐酸浓度不同时,漂白粉与盐酸混合发生反应的类型不同。
漂白粉与稀盐酸发生复分解反应,化学方程式为_________________________。漂白粉与浓盐酸发生氧化还原反应,化学方程式为____________________________________。
(2)氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
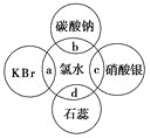
①能证明氯水具有漂白性的是______(填“a”“b”“c”或“d”)。
②c过程中的现象是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B![]() 3C+4D反应中,表示该反应速率最快的是( )
3C+4D反应中,表示该反应速率最快的是( )
A.v(A)=0.5mol·L-1·s-1B.v(B)=0.3mol·L-1·s-1
C.v(C)=0.3mol·L-1·s-1D.v(D)=1mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新能源汽车上有一种质子交换膜燃料电池,其工作原理如图所示,下列叙述正确的( )
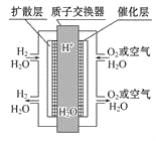
A.通入氧气的电极发生氧化反应
B.通入氢气的电极为正极
C.总反应式为O2+2H2![]() 2H2O
2H2O
D.正极的电极反应式为O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O)呈淡黄色,可用作晒制蓝图。某实验小组对纯净草酸亚铁晶体热分解气体产物成分的进行探究。小组成员采用如图装置(可重复选用)进行实验:
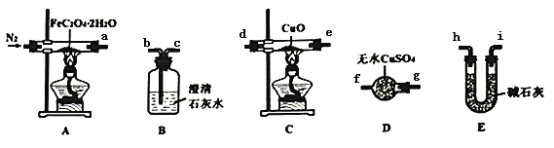
请回答下列问题:
(1)E中盛装碱石灰的仪器名称为___。
(2)D中的现象是___,是为了证明草酸亚铁晶体分解产物中可能含有___。
(3)按照气流从左到右的方向,上述装置的接口顺序为a→g→f→___→尾气处理装置(仪器可重复使用)。
(4)实验前先通入一段时间N2,其目的为___。
(5)实验证明了气体产物中含有CO,依据的实验现象为___。
(6)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种常用的化工原料,经常可以用来转化成高附加值的CO、CH4、CH3OH、CO(NH2)2等一碳(C1)产物。
Ⅰ.以CO2与NH3为原料可以合成尿素[CO(NH2)2]。合成尿素的反应为2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)。在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率的变化情况如图所示。该反应的ΔH___(填“>”、“<”或“=”,下同)0,若y表示压强,则y1___y2,若y表示反应开始时的氨碳比[
CO(NH2)2(s)+H2O(g)。在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率的变化情况如图所示。该反应的ΔH___(填“>”、“<”或“=”,下同)0,若y表示压强,则y1___y2,若y表示反应开始时的氨碳比[![]() ],则y1__y2。
],则y1__y2。

Ⅱ.CO2加氢过程,主要发生的三个竞争反应为:
反应i:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) H=-49.01kJmol-1
CH3OH(g)+H2O(g) H=-49.01kJmol-1
反应ii:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) H=-165.0kJmol-1
CH4(g)+2H2O(g) H=-165.0kJmol-1
反应iii:CO2(g)+H2(g)![]() CO(g)+H2O(g) H=+41.17kJmol-1
CO(g)+H2O(g) H=+41.17kJmol-1
回答下列问题:(1)由CO、H2合成甲醇的热化学方程式为__。
(2)如图是某甲醇燃料电池工作的示意图。

质子交换膜(只有质子能够通过)左右两侧的溶液均为1L2mol·L-1H2SO4溶液。电极a上发生的电极反应为___,当电池中有1mole发生转移时左右两侧溶液的质量之差为___g(假设反应物耗尽,忽略气体的溶解)。
(3)我国科学家研究了不同反应温度对含碳产物组成的影响。在反应器中按![]() =3∶1通入H2和CO2,分别在0.1MPa和1MPa下进行反应。试验中温度对平衡组成C1(CO2、CO、CH4)中的CO和CH4的影响如图所示(该反应条件下甲醇产量极低,因此忽略“反应i”):
=3∶1通入H2和CO2,分别在0.1MPa和1MPa下进行反应。试验中温度对平衡组成C1(CO2、CO、CH4)中的CO和CH4的影响如图所示(该反应条件下甲醇产量极低,因此忽略“反应i”):
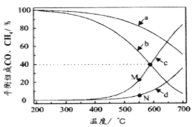
则表示1MPa时CH4和CO平衡组成随温度变化关系的曲线分别是___、___。M点所表示物质的平衡组成高于N点的原因是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com