
| A. | 1.12L | B. | 0.56L | C. | 0.448L | D. | 0.224L |
分析 n(Cu)=$\frac{1.92g}{64g/mol}$=0.03mol,铜粉完全作用时,用排水法收集的气体为NO,由电子守恒及V=nVm计算.
解答 解:铜粉与一定量的浓硝酸反应,当铜粉完全作用时,用排水法收集的气体为NO,整个过程中Cu失去电子,N得到电子,由电子守恒可知,n(NO)=$\frac{0.03mol×(2-0)}{(5-2)}$=0.02mol,其体积为0.02mol×22.4L/mol=0.448L,故选C.
点评 本题考查氧化还原反应的计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与计算能力的考查,注意电子守恒的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 元素周期表有7个横行,7个周期 | B. | 元素周期表有16个纵行,16个族 | ||
| C. | ⅠA 族的元素全部是金属元素 | D. | 0族元素的原子最外层都有8个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
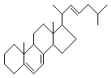
| A. | 属于芳香族化合物 | |
| B. | 分子式为C27H42 | |
| C. | 核磁共振氢谱证明分子中的5个甲基上的氢原子化学环境相同 | |
| D. | 不能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.12L | B. | 3.36L | C. | 4.48L | D. | 6.72L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
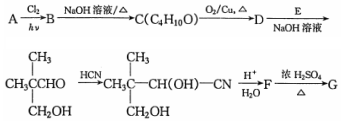
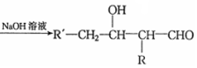
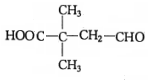
 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$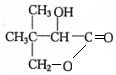 +H2O.F能发生缩聚反应,则生成链节的主链上有四个碳愿子的高分子化合物的结构简式为
+H2O.F能发生缩聚反应,则生成链节的主链上有四个碳愿子的高分子化合物的结构简式为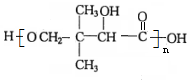 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
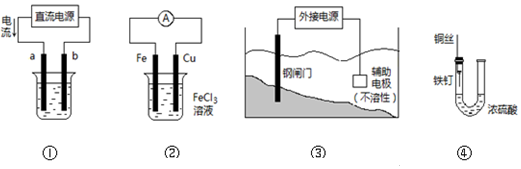
| A. | 用装置①精炼铜,则b为粗铜,电解质溶液为CuSO4溶液 | |
| B. | 装置②的总反应是:Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 装置③中钢闸门应与外接电源的负极相连被保护,该方法叫做牺牲阳极的阴极保护法 | |
| D. | 装置④中的铁钉不容易被腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com