

| a | b | c | d | |
| ¢ń | øÉŌļµÄÓŠÉ«²¼Ģõ | øÉŌļµÄÓŠÉ«²¼Ģõ | ŹŖČóµÄÓŠÉ«²¼Ģõ | ŹŖČóµÄÓŠÉ«²¼Ģõ |
| ¢ņ | ¼īŹÆ»Ņ | ¹č½ŗ | ÅØĮņĖį | ĪŽĖ®ĀČ»ÆøĘ |
| ¢ó | ŹŖČóµÄÓŠÉ«²¼Ģõ | ŹŖČóµÄÓŠÉ«²¼Ģõ | øÉŌļµÄÓŠÉ«²¼Ģõ | øÉŌļµÄÓŠÉ«²¼Ģõ |
·ÖĪö £Ø1£©ĘÆ°×¾«µÄÓŠŠ§³É·ÖŹĒ“ĪĀČĖįøĘ£¬“ĪĀČĖįøĘÓėÅØŃĪĖį·“Ӧɜ³ÉĀČ»ÆøĘ”¢ĀČĘųÓėĖ®£»
£Ø2£©ŃĪĖįŅ×»Ó·¢£¬·“Ó¦ÖĘČ”µÄĀČĘųÖŠŗ¬ÓŠĀČ»ÆĒā£¬ĀČ»ÆĒāŅ×ČÜÓŚĖ®£¬ĀČĘųŌŚ±„ŗĶŹ³ŃĪĖ®ÖŠČܽā¶Č²»“ó£»
×°ÖĆBŅąŹĒ°²Č«Ę棬¼ą²āŹµŃé½ųŠŠŹ±CÖŠŹĒ·ń·¢Éś¶ĀČū£¬·¢Éś¶ĀČūŹ±BÖŠµÄ£¬Ń¹ĒæŌö“ó£»
£Ø3£©ĪŖĮĖŃéÖ¤ĀČĘųŹĒ·ń¾ßÓŠĘư׊Ō£¬ŅŖŃéÖ¤øÉŌļĀČĘųĪŽĘư׊Ō£¬ŹŖČóµÄÓŠÉ«²¼ĢõÖŠ£¬ĀČĘųŗĶĖ®·“Ӧɜ³É“ĪĀČĖį¾ßÓŠĘư׊Ō£»
£Ø4£©ĶعżÖĆ»»·“Ó¦æÉŃéÖ¤ĀČĘų”¢ä唢µāµÄŃõ»ÆŠŌĒæČõ£¬±Č½ĻĀČ”¢ä唢µāµÄ·Ē½šŹōŠŌ£»
£Ø5£©“ņæŖ»īČū£¬½«×°ÖĆDÖŠÉŁĮæČÜŅŗ¼ÓČė×°ÖĆEÖŠ£¬Éś³ÉµÄäåµ„ÖŹŗĶµā»Æ¼Ų·“Ӧɜ³Éµāµ„ÖŹ£¬µāµ„ÖŹČܽāÓŚ±½ÖŠ£¬Õńµ“·Ö²ć£¬±½²ćŌŚÉĻ²ć£»
£Ø6£©ĀČĘų¾ßÓŠĒæŃõ»ÆŠŌ£¬ŌŚČÜŅŗÖŠ½«SO32-Ńõ»ÆSO42-Ķ¬Ź±Éś³ÉCl-”¢H+£®ČōøÄÓĆNaHSO3£¬»į·¢Éś·“Ó¦4HSO3-+Cl2=SO42-+2Cl-+3SO2”ü+2H2O£¬Éś³É¶žŃõ»ÆĮņĘųĢ壮
½ā“š ½ā£ŗ£Ø1£©ĘÆ°×¾«µÄÓŠŠ§³É·ÖŹĒ“ĪĀČĖįøĘ£¬“ĪĀČĖįøĘÓėÅØŃĪĖį·“Ó¦µÄ·“Ó¦·½³ĢŹ½ĪŖ£ŗCa£ØClO£©2+4HCl£ØÅØ£©ØTCaCl2+2Cl2”ü+2H2O£¬
¹Ź“š°øĪŖ£ŗCa£ØClO£©2£¬Ca£ØClO£©2+4HCl£ØÅØ£©ØTCaCl2+2Cl2”ü+2H2O£»
£Ø2£©ŃĪĖįŅ×»Ó·¢£¬·“Ó¦ÖĘČ”µÄĀČĘųÖŠŗ¬ÓŠĀČ»ÆĒā£¬ĀČ»ÆĒāŅ×ČÜÓŚĖ®£¬ĀČĘųŌŚ±„ŗĶŹ³ŃĪĖ®ÖŠČܽā¶Č²»“ó£¬B×°ÖĆæÉŅŌ³żČ„Cl2ÖŠHCl£»
×°ÖĆBŅąŹĒ°²Č«Ę棬¼ą²āŹµŃé½ųŠŠŹ±CÖŠŹĒ·ń·¢Éś¶ĀČū£¬·¢Éś¶ĀČūŹ±BÖŠµÄ£¬Ń¹ĒæŌö“ó£¬BÖŠ³¤¾±Ā©¶·ÖŠŅŗĆęÉĻÉż£¬ŠĪ³ÉĖ®Öł£»
¹Ź“š°øĪŖ£ŗ³żČ„Cl2ÖŠHCl£»BÖŠ³¤¾±Ā©¶·ÄŚŅŗĆęÉĻÉż£¬ŠĪ³ÉŅ»¶ĪĖ®Öł£¬×¶ŠĪĘæÄŚŅŗĆęĻĀ½µ£»
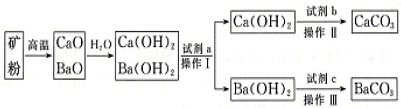
£Ø3£©×°ÖĆCµÄŹµŃéÄæµÄŹĒŃéÖ¤ĀČĘųŹĒ·ń¾ßÓŠĘư׊Ō£¬ŃéÖ¤ĀČĘųŹĒ·ń¾ßÓŠĘư׊Ō£¬ŅŖŃéÖ¤øÉŌļĀČĘųĪŽĘư׊Ō£¬ŹŖČóµÄÓŠÉ«²¼ĢõÖŠ£¬ĀČĘųŗĶĖ®·“Ӧɜ³É“ĪĀČĖį¾ßÓŠĘư׊Ō£¬Ń”ĻīÖŠabcµÄ¢ņÖŠ¶¼ŹĒøÉŌļ¼Į£¬ŌŁĶØČėŹŖČóµÄÓŠÉ«²¼Ģõ²»ÄÜŃéÖ¤ĀČĘųµÄĘư׊Ō£¬ĖłŅŌCÖŠI”¢II”¢IIIŅĄ“Ī·ÅČėŹŖČóµÄÓŠÉ«²¼Ģõ”¢ĪŽĖ®ĀČ»ÆøĘ”¢øÉŌļµÄÓŠÉ«²¼Ģõ£¬ĖłŅŌŃ”d£¬
¹Ź“š°øĪŖ£ŗd£»
£Ø4£©ŅĄ¾ŻĀČĘųŗĶäå»ÆÄĘ·“Ӧɜ³Éäåµ„ÖŹ£¬ŅŗĢåäåµ„ÖŹŗĶµā»Æ¼ŲČÜŅŗÖŠµÄµā»Æ¼Ų·“Ӧɜ³Éµāµ„ÖŹ£¬ŅĄ¾ŻĀČĘų”¢ä唢µāµ„ÖŹÖ®¼äµÄÖĆ»»·“Ó¦£¬æÉŅŌÅŠ¶ĻĀČ”¢ä唢µāµÄ·Ē½šŹōŠŌĒæČõ£»
¹Ź“š°øĪŖ£ŗ±Č½ĻĀČ”¢ä唢µāµÄ·Ē½šŹōŠŌĒæČõ£»
£Ø5£©“ņæŖ»īČū£¬½«×°ÖĆDÖŠŗ¬äåµ„ÖŹµÄÉŁĮæČÜŅŗ¼ÓČėģŹµā»Æ¼ŲŗĶ±½µÄ×°ÖĆEÖŠ£¬äåµ„ÖŹŗĶµā»Æ¼Ų·“Ӧɜ³Éµāµ„ÖŹ£¬µāµ„ÖŹČÜÓŚ±½³Ź×ĻŗģÉ«£¬Õńµ“£®¹Ū²ģµ½µÄĻÖĻóŹĒ£ŗEÖŠČÜŅŗ·ÖĪŖĮ½²ć£¬ÉĻ²ć£Ø±½²ć£©ĪŖ×ĻŗģÉ«£¬
¹Ź“š°øĪŖ£ŗEÖŠČÜŅŗ·ÖĪŖĮ½²ć£¬ÉĻ²ć£Ø±½²ć£©ĪŖ×ĻŗģÉ«£»
£Ø6£©ĀČĘų¾ßÓŠĒæŃõ»ÆŠŌ£¬ŌŚČÜŅŗÖŠ½«SO32-Ńõ»ÆSO42-Ķ¬Ź±Éś³ÉCl-”¢H+£¬·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖSO32-+Cl2+H2O=SO42-+2Cl-+2H+£¬ČōøÄÓĆNaHSO3£¬»į·¢Éś·“Ó¦HSO3-+Cl2+H2O=SO42-+2Cl-+3H+»ņ4HSO3-+Cl2=SO42-+2Cl-+3SO2”ü+2H2O£¬Éś³É¶žŃõ»ÆĮņĘųĢ壬¶žŃõ»ÆĮņĪŪČ¾»·¾³£¬ĖłŅŌ²»ÄÜÓĆNaHSO3“śĢęNa2SO3£¬
¹Ź“š°øĪŖ£ŗHSO3-+Cl2+H2O=SO42-+2Cl-+3H+»ņ4HSO3-+Cl2=SO42-+2Cl-+3SO2”ü+2H2O£»·ń£®
µćĘĄ ±¾Ģāæ¼²éĮĖĀČĘųŹµŃéŹŅÖĘČ””¢ĀČĘų»ÆѧŠŌÖŹ”¢ŹµŃéÉč¼Ę”¢ŹµŃé×°ÖƵĥķ½āĘĄ¼Ū”¢»Æѧ·½³ĢŹ½µÄŹéŠ“µČ£¬ŹĒ¶ŌĖłŃ§ÖŖŹ¶µÄ×ŪŗĻŌĖÓĆ£¬×¢Ņā»ł“”ÖŖŹ¶µÄÕĘĪÕ£¬±¾ĢāÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| 0”ę | 50”ę | 80”ę | |
| Ca£ØOH£©2 | 0.173g | 0.13g | 0.094g |
| Ba£ØOH£©2•8H2O | 1.64g | 13.2g | 101.4g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ź±¼ä/min | CO | H2O£Øg£© | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 20æĖ | B£® | 40æĖ | C£® | 48æĖ | D£® | 36æĖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬48gO2ŗĶO3ŗ¬ÓŠµÄŃõŌ×ÓŹż¾łĪŖ3NA5.4gĀĮÓė×ćĮæNaOH·“Ó¦×ŖŅʵĵē×ÓŹżĪŖ0.3NA | |
| B£® | 12gÖŲĖ®£ØD2O£©ÖŠŗ¬ÓŠµÄµē×ÓŹżĪŖ6 NA | |
| C£® | ±ź×¼×“æöĻĀ£¬11.2L±½Ėłŗ¬Ō×ÓŹżĪŖ6NA | |
| D£® | 160gµØ·ÆČÜÓŚĖ®ŠĪ³É1LČÜŅŗ£¬ČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ1mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ca£ØOH£©2ØTCa2++2OH- | B£® | ¾Ę¾«£ŗCH3CH2OHØTCH3CH2O-+H+ | ||
| C£® | BaCl2ØTBa2++Cl${\;}_{2}^{2-}$ | D£® | H2SO4$\frac{\underline{\;Ķصē\;}}{\;}$2H++SO${\;}_{4}^{2-}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | ||
| C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com