
分析 I.(1)食醋的物质的量浓度为0.7mol•L-1,总酸量为0.75mol•L-1×60g/mol=45g/L;
(2)醋酸与碳酸钙反应生成醋酸钙、水和二氧化碳;
II、(1)根据配制一定物质的量浓度的溶液的步骤是计算、量取、稀释、移液、洗涤、定容、摇匀选择合适的仪器;
(2)求出浓盐酸的物质的量浓度c=$\frac{1000ρω}{M}$,然后根据稀释定律C浓V浓=C稀V稀来计算;
(3)根据c=$\frac{n}{V}$,通过判断不当操作对溶质的物质的量n和溶液体积V的影响来分析误差;
III.(1)溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现光亮光路,为丁达尔现象;
(2)胶体遇电解质溶液发生聚沉;
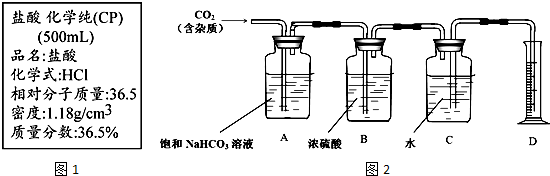
IV.(1)CO2用排水法收集,在收集之前不需要对气体进行干燥;
(2)盐酸易挥发,生成的CO2气体中含有挥发出的氯化氢气体,A装置中的饱和NaHCO3溶液可以吸收氯化氢;
(3)实验前测得C装置(含水)重量为50.00g,实验完毕后C装置(含水)重量为40.02g,D中量筒读数为10.0 mL,这说明收集到CO2的质量=40.02g+10.0g-50.0g=0.02g,其体积是10.0ml,所以CO2的密度=$\frac{0.02g}{0.01L}$=2g/L;已知H2密度为0.09g/L(以上数据均已折合为标况下数值),则根据在相同条件下气体的密度之比等于相对分子质量之比可知可计算出二氧化碳的相对分子质量.
解答 解:I.(1)食醋的物质的量浓度为0.75mol•L-1,总酸量为0.75mol•L-1×60g/mol=45g/L,即4.50g/100mL,为酿造醋,
故答案为:4.50;酿造;
(2)醋酸与碳酸钙反应生成醋酸钙、水和二氧化碳,离子方程式:2CH3COOH+CaCO3=2CH3COO-+CO2↑+H2O+Ca2+,
故答案为:2CH3COOH+CaCO3=2CH3COO-+CO2↑+H2O+Ca2+;
II.(1)根据配制一定物质的量浓度的溶液的步骤是计算、量取、稀释、移液、洗涤、定容、摇匀可知需要的仪器有:量筒、烧杯、玻璃棒、100mL容量瓶和胶头滴管,故需要选用的仪器有①③⑤⑦,还缺少的仪器有100mL容量瓶,
故答案为:100mL容量瓶;
(2)浓盐酸的物质的量浓度c=$\frac{1000×1.18×36.5%}{36.5}$mol/L=11.8mol/L,设需要的浓盐酸的体积为VmL,然后根据稀释定律c浓V浓=c稀V稀可知:
11.8mol/L×VmL=100mL×1mol•L-1,解得V=8.5mL,
故答案为:8.5;
(3)A.定容时俯视容量瓶刻度线,会导致溶液体积偏小,则浓度偏高,故A错误;
B.容量瓶在使用前未干燥,里面有少量蒸馏水,对浓度无影响,故B错误;
C.转移溶液后,未洗涤烧杯和玻璃棒,会导致溶质的损失,则浓度偏低,故C正确;
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线,则溶液体积增加,所配浓度偏小,故D正确;
故答案为:CD;
III.(1)胶体能产生丁达尔效应,鸡蛋的蛋清配制成溶液属于胶体,因此用激光笔照射溶液,可以发现一条光束穿过鸡蛋清溶液,此现象称为丁达尔效应,
故答案为:丁达尔效应;
(2)胶体和电解质混合可以聚沉.盐酸是电解质氯化氢的水溶液,所以将配制好的盐酸溶液加入到鸡蛋清溶液中,会出现絮状沉淀,此现象称为胶体的聚沉,
故答案为:胶体的聚沉;
IV.(1)根据装置可知,CO2用排水法收集,因此在收集之前不需要对气体进行干燥,即没有必要设计B装置,
故答案为:无;排水法收集气体,不需要对气体进行干燥;
(2)由于盐酸易挥发,因此生成的CO2气体中含有挥发出的氯化氢气体,所以A装置中的饱和NaHCO3溶液的作用是吸收氯化氢,
故答案为:吸收(除去)CO2中混有的HCl杂质;
(3)实验前测得C装置(含水)重量为50.00g,实验完毕后C装置(含水)重量为40.02g,D中量筒读数为10.0 mL,这说明收集到CO2的质量=40.02g+10.0g-50.0g=0.02g,其体积是10.0ml,所以CO2的密度为:$\frac{0.02g}{0.01L}$=2g/L;
已知H2密度为0.09g/L(以上数据均已折合为标况下数值),
在相同条件下气体的密度之比等于相对分子质量之比,
所以CO2的相对分子质量为:$\frac{2}{0.09}$×2=44.4,
故答案为:44.4.
点评 本题考查了性质实验方案的设计,题目难度中等,涉及配置一定物质的量浓度的溶液方法及误差分析、化学计算、胶体的性质、离子方程式书写等知识,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及化学实验、进行计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
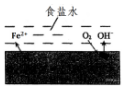 在一块表面无锈的铁片上滴食盐水,放置一段时间后看到铁片上有铁锈出现.铁片腐蚀过程中发生的总化学方程式:2Fe+2H2O+O2═2Fe(OH)2,Fe(OH)2进一步被氧气氧化为Fe(OH)3,再在一定条件下脱水生成铁锈,其原理如图.下列说法正确的是( )
在一块表面无锈的铁片上滴食盐水,放置一段时间后看到铁片上有铁锈出现.铁片腐蚀过程中发生的总化学方程式:2Fe+2H2O+O2═2Fe(OH)2,Fe(OH)2进一步被氧气氧化为Fe(OH)3,再在一定条件下脱水生成铁锈,其原理如图.下列说法正确的是( )| A. | 铁片发生还原反应而被腐蚀 | |
| B. | 此过程中电子从C移向Fe | |
| C. | 铁片腐蚀中负极发生的电极反应:2H2O+O2+4e-═4OH- | |
| D. | 铁片里的铁和碳与食盐水形成无数微小原电池,发生了电化学腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度(℃) | 0 | 20 | 60 |
| K2SO4溶解的量(g) | 7.4 | 11.1 | 18.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/K CO2转化率% $\frac{n({H}_{2})}{n(C{O}_{2})}$ | 500 | 600 | 700 | 800 |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
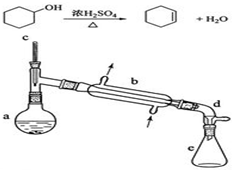 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环已醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环已烯 | 82 | 0.8102 | 83 | 难溶于水 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 图象法是研究化学反应的焓变的一种常用方法.已知化学反应A2(g)+B2(g)═2AB(g)的能量变化曲线如图所示,则下列叙述中正确的是( )
图象法是研究化学反应的焓变的一种常用方法.已知化学反应A2(g)+B2(g)═2AB(g)的能量变化曲线如图所示,则下列叙述中正确的是( )| A. | 每生成2 mol AB时吸收(a-b) kJ能量 | |
| B. | 该反应热△H=+(a-b) kJ•mol-1 | |
| C. | 该反应中反应物的总能量高于生成物的总能量 | |
| D. | 断裂1 mol A-A和1 mol B-B键时放出a kJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用可见光束可以鉴别红褐色的氢氧化铁胶体和溴水,是因为溶液与胶体的本质区别是能否发生丁达尔效应 | |
| B. | 分散系是一种物质分散到另一种物质中形成的混合体系 | |
| C. | 氢氧化铁胶体具有吸附性,能吸附水中悬浮颗粒并沉降,因而常用于净水 | |
| D. | 淀粉溶液和蛋白质溶液是溶液,不可能是胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com