
| A. | 将饱和食盐水滴入盛有电石的烧瓶中制乙炔 | |
| B. | 将乙醛滴入银氨溶液中,加热煮沸制银镜 | |
| C. | 用乙醇与3mol•L-1的H2SO4混合共热到170℃以上制乙烯 | |
| D. | 向氯仿中加入NaOH溶液,加热充分反应后,再加入AgNO3溶液,若观察到白色沉淀即可证明氯仿中含有氯元素 |
分析 A.为减缓反应的速率,可用饱和食盐水与电石反应;
B.银镜反应要在水浴加热的条件下进行;
C.乙醇的消去反应中,必须使用浓硫酸;
D.向氯仿中加入NaOH溶液,加热充分反应后,发生水解,应调节至酸性再加AgNO3检验氯离子.
解答 解:A.电石与水水制取乙炔的反应中,为减缓反应的速率,可用饱和食盐水与电石反应,故A正确;
B.银镜反应要在水浴加热的条件下,将乙醛滴入银氨溶液中,加热煮沸得到黑色沉淀,故B错误;
C.3mol•L-1的H2SO4为稀硫酸,而乙醇的消去反应中必须使用浓硫酸,故C错误;
D.向氯仿中加入NaOH溶液,加热充分反应后,发生水解,应加硝酸调节至酸性再加AgNO3检验氯离子,否则不能检验氯离子,碱溶液中OH-与AgNO3反应,故D错误;
故选A.
点评 本题考查化学实验方案的评价,题目难度中等,涉及溶液的配制、滴定实验操作、酯的水解及除杂、离子的检验等,注重实验操作和细节的考查,注意掌握常见物质的性质,试题培养了学生的分析能力及化学实验能力.


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A和M原子的最外层电子数之差不一定为5 | |
| B. | A和M原子的最外层电子数之和一定为7 | |
| C. | A和M原子的电子数之差一定为11 | |
| D. | A和M的原子序数之差不一定为5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应不一定是吸收热量的反应 | |
| B. | 科学家经常在金属与非金属的交界线处寻找良好的半导体材料 | |
| C. | 催化剂是影响化学反应速率和化学平衡的一个重要因素 | |
| D. | 物质燃烧可看做“储存”在物质内部的能量(化学能)转化为热能释放出来 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
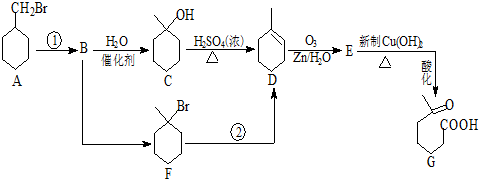
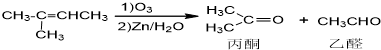
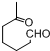 +NaOH+2Cu(OH)2$\stackrel{△}{→}$
+NaOH+2Cu(OH)2$\stackrel{△}{→}$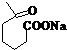 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.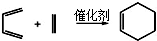
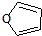 )也可以发生“Diels-Alder反应”,该化学方程式为:
)也可以发生“Diels-Alder反应”,该化学方程式为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该微粒的质量数为2 | |
| B. | 该微粒不显电性 | |
| C. | 它与普通中子互称为同位素 | |
| D. | 在元素周期表中与氢元素占同一位置 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com