
| A、O2和O3的混合气体共6.4g,其中所含氧原子数一定为0.4NA |
| B、常温常压下,22.4L二氧化碳含有的原子总数为3NA |
| C、将标准状况下22.4L NO与11.2L O2混合后所含分子数为1.5NA |
| D、物质的量浓度为0.25mol?L-1的MgCl2溶液中含有Cl个数为0.5NA |
| m |
| M |
| 6.4g |
| 16g/mol |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
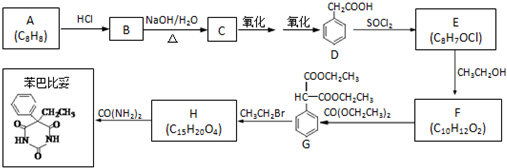
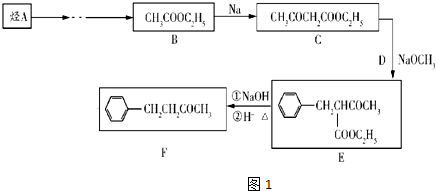
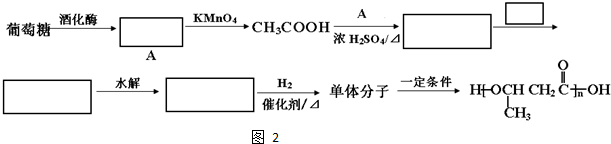
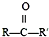 (R、R′代表烷基或H原子)发生缩合反应生成新的有机物和水.苯酚还能发生如下反应生成有机酸酯:
(R、R′代表烷基或H原子)发生缩合反应生成新的有机物和水.苯酚还能发生如下反应生成有机酸酯: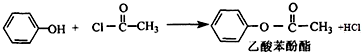
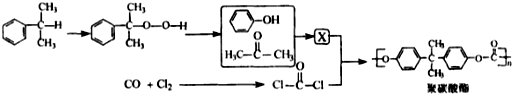
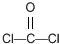 反应合成聚碳酸酯的化学方程式:
反应合成聚碳酸酯的化学方程式: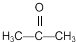 的同分异构体与新制银氨溶液发生反应的化学方程式:
的同分异构体与新制银氨溶液发生反应的化学方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
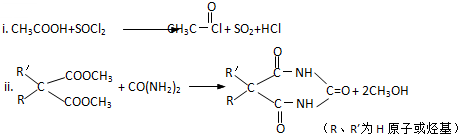
查看答案和解析>>
科目:高中化学 来源: 题型:
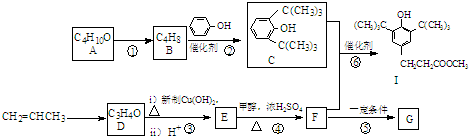

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
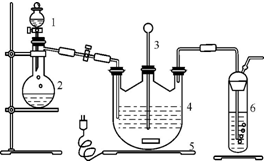 硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得:Na2SO3+S
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得:Na2SO3+S
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4:9 | B、1:1 |
| C、7:6 | D、4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 杂质 | 除杂所用试剂和方法 | |
| A | CO2 | CO | 在氧气中点燃 |
| B | NaHCO3溶液 | Na2CO3 | 通过量的CO2 |
| C | Cu | Fe | 加稍过量稀盐酸溶解、过滤 |
| D | KCl | I2 | 加热 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com