
| A. | 用湿润的红色石蕊试纸检验某种气体是否是NH3 | |
| B. | 某种有色溶液可使淀粉-KI试纸变蓝色,则该溶液中可能含有Fe3+ | |
| C. | 用玻璃棒蘸取溶液点在用蒸馏水湿润过的pH试纸上可测量该溶液的pH | |
| D. | 将湿润的蓝色石蕊试纸片粘在玻璃棒上置于氯气中,试纸先变红后褪色 |
分析 A.氨气是碱性气体,遇到湿润的红色石蕊试纸变蓝;
B.铁离子可以优惠碘离子生成碘单质;
C.用蒸馏水湿润过的pH试纸会稀释溶液;
D.将湿润的蓝色石蕊试纸片粘在玻璃棒上置于氯气中,氯气和水反应生成盐酸和次氯酸.
解答 解:A.氨气是碱性气体,遇到湿润的红色石蕊试纸变蓝,用湿润的红色石蕊试纸检验某种气体是否是NH3,故A正确;
B.铁离子可以氧化碘离子生成碘单质,2Fe3++2I-=2Fe2++I2,某种有色溶液可使淀粉-KI试纸变蓝色,则该溶液中可能含有Fe3+,故B正确;
C.用蒸馏水湿润过的pH试纸会稀释溶液,用玻璃棒蘸取溶液点在用蒸馏水湿润过的pH试纸上测量该溶液的pH,酸溶液变大、碱溶液变小,强酸强碱盐溶液不变,故C错误;
D.将湿润的蓝色石蕊试纸片粘在玻璃棒上置于氯气中,氯气和水反应生成盐酸和次氯酸,盐酸使试纸变红色,次氯酸具有漂白性,能使变红色的试纸褪色,试纸先变红后褪色,故D正确;
故选C.
点评 本题考查了试纸的使用方法,注意检验气体和检验溶液的使用方法,掌握基础是解题关键,题目难度不大.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
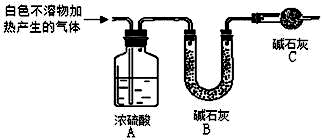
| 实验序号 | 实验 | 实验现象 | 结论 |
| 实验Ⅰ | 取一小段镁条,用砂纸擦去表面氧化膜,将其放入足量的滴有酚酞的饱和NaHCO3溶液中,充分反应后过滤 | 产生较多气泡和白色不溶物,溶液有浅红色变成红色 | |
| 实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧,火焰呈淡蓝色 | 气体成分为 ①氢气 |
| 实验Ⅲ | 取实验Ⅰ中白色不溶物滤出、洗涤,取少量加入足量稀盐酸 | ②产生气泡沉淀全部溶解 | 白色不溶物中含有 MgCO3 |
| 实验Ⅳ | ③CaCl2或BaCl2 | 产生白色沉淀,溶液红色变浅 | 溶液中存在CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
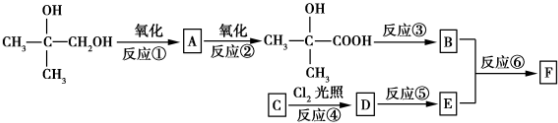
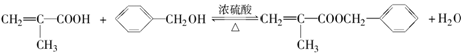 .
.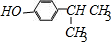 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
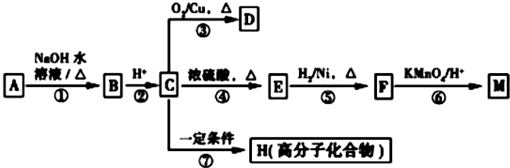
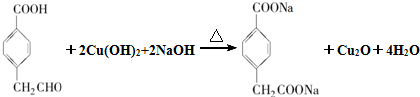
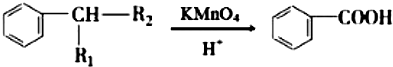 (R1、R2表示烃基或氢原子)
(R1、R2表示烃基或氢原子)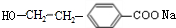 .
.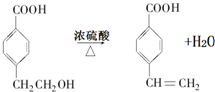 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ②③④⑤⑥ | C. | ②③⑤⑥⑦ | D. | ①②⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)有两种气体单质Am和Bn.已知7.2g Am和6.3g Bn所含的原子个数相同,分子个数之比却为2:3.又知A原子中L电子层含电子数是K电子层的3倍.通过计算回答:写出B的元素名称氮
(1)有两种气体单质Am和Bn.已知7.2g Am和6.3g Bn所含的原子个数相同,分子个数之比却为2:3.又知A原子中L电子层含电子数是K电子层的3倍.通过计算回答:写出B的元素名称氮查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用消毒液杀灭游泳池中的藻类 | |
| B. | 用CaCl2融化路面的积雪 | |
| C. | 用石灰修复被酸雨浸蚀的土壤 | |
| D. | 用催化剂将汽车尾气中的CO和NO转化为无害物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com