
| A. | 常温下浓硫酸能使铝发生钝化,可在常温下用铝制贮罐贮运浓硫酸 | |
| B. | 取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ | |
| C. | 检验Fe(NO3)2晶体是否已氧化变质,将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 | |
| D. | 常温下将Al片放入浓硝酸中,无明显变化,所以Al与浓硝酸不反应 |
分析 A.浓硫酸具有强的氧化性,常温下能够使铝发生钝化;
B.验证亚铁离子的存在,首先应排除铁离子干扰,正确顺序是先加入硫氰化钾观察现象后再滴加氯水;
C.硝酸根离子在酸性环境下具有强的氧化性,能够氧化二价铁离子;
D.浓硝酸具有强的氧化性,常温下能够使铝发生钝化;
解答 解:A.浓硫酸具有强的氧化性,常温下能够使铝发生钝化,生成致密氧化膜,阻止反应继续进行,所以可在常温下用铝制贮罐贮运浓硫酸,故A正确;
B.验证亚铁离子的存在,首先应排除铁离子干扰,正确顺序是先加入硫氰化钾观察现象后再滴加氯水,故B错误;
C.将Fe(NO)2样品溶于稀H2SO4后,酸性条件下,NO3-能把Fe2+氧化为Fe3+,滴加KSCN溶液变红,不能说明Fe(NO3)2晶体已经变质,故C错误;
D.浓硝酸具有强的氧化性,常温下能够使铝发生钝化,钝化属于化学反应,故D错误;
故选:A.
点评 本题考查了元素化合物知识,熟悉浓硫酸、浓硝酸的性质是解题关键,注意三价铁离子、二价铁离子检验,注意钝化属于化学反应,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去CO2中少量O2:用点燃的方法 | |
| B. | 除去NaCl溶液中的Na2SO4:加入适量Ba(NO3)2溶液后,过滤 | |
| C. | 除去Cu中的少量Fe:加入足量稀硫酸溶液后,过滤,洗涤,干燥 | |
| D. | 除去CO2中的少量HCl:通入NaOH溶液后,收集气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
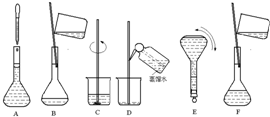 如图表示配制 100mL 0.100ol•L-1 Na2CO3溶液的几个关键实验步骤和操作,据图回答下列问题:
如图表示配制 100mL 0.100ol•L-1 Na2CO3溶液的几个关键实验步骤和操作,据图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60% | B. | 40% | C. | 33.3% | D. | 66.7% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常用作净水剂的KAl(SO4)2和漂白粉都是强电解质 | |
| B. | 氯气溶于水生成的次氯酸具有强氧化性,可以起到除去水中杂质和杀菌消毒作用 | |
| C. | 氮氧化物可以破坏臭氧层,也能形成酸雨 | |
| D. | “玉兔”月球车太阳能电池板可将光能转换为电能,所用转换材料是二氧化硅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com