
【题目】Ⅰ.如何降低大气中CO2的含量及有效利用CO2,目前已引起各国普遍重视。
(1)工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1molCO2和3molH2,在500℃下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。实验测得CO2(g)和CH3OH(g)的浓度随时间变化如图1所示。
CH3OH(g)+H2O(g)。实验测得CO2(g)和CH3OH(g)的浓度随时间变化如图1所示。

①从反应开始到平衡,氢气的平均反应速率v(H2)=__;
②图2是改变温度时H2的化学反应速率随时间变化的示意图,则该反应的正反应是__热(填“吸”或“放”)反应。
③该反应的平衡常数K为__(保留两位小数)。若提高温度到800℃进行,达平衡时,K值__(填“增大”、“减小”或“不变”),
④500℃达平衡时,CH3OH的体积分数ω为__。
Ⅱ.(2)工业上可利用煤的气化产物(CO和H2)合成二甲醚(CH3OCH3),其三步反应如下:
①2H2(g)+CO(g)![]() CH3OH(g) △H=-90.8kJmol-1
CH3OH(g) △H=-90.8kJmol-1
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H=-23.5kJmol-1
CH3OCH3(g)+H2O(g) △H=-23.5kJmol-1
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41.3kJmol-1
CO2(g)+H2(g) △H=-41.3kJmol-1
总合成反应的热化学方程式为__。
(3)一定条件下的密闭容器中,上述总反应达到平衡时,要提高CO的转化率,可以采取的措施是__(填字母代号)。
A.高温高压
B.加入催化剂
C.减少CO2的浓度
D.增加CO的浓度
E.分离出二甲醚
(4)已知反应②2CH3OH(g)![]() CH3OCH3(g)+H2O(g)在某温度下的平衡常数K=400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)在某温度下的平衡常数K=400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
c/molL-1 | 0.44 | 0.60 | 0.60 |
此时,v(正)__v(逆)(填“>”、“<”或“=”)。
【答案】0.225 molL-1min-1 放 5.33 减小 30% 3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g) △H=-246.4kJ/mol CE >
CH3OCH3(g)+CO2(g) △H=-246.4kJ/mol CE >
【解析】
(1)①分析图1,在10min时CO2、CH3OH的浓度不再发生变化,说明此时反应达到平衡状态,可先求出CO2的速率,根据同一反应中,各物质的速率之比等于其化学计量数之比,求出H2的速率。
②分析图2,在t2时,改变温度,v'正、v'逆突然增大,且v'正<v'逆,可知改变的条件为升高温度,此时反应向逆反应方向移动,据此分析反应是吸热还是放热反应。
(1)①由图可知,10min到达平衡时二氧化碳的浓度变化量为1.00mol/L-0.25mol/L=0.75mol/L,所以v(CO2)=![]() ,根据同一反应中,各物质的速率之比等于其化学计量数之比,可知v(H2)=3v(CO2)=3×0.075molL-1min-1=0.225 molL-1min-1,故答案为:0.225 molL-1min-1;
,根据同一反应中,各物质的速率之比等于其化学计量数之比,可知v(H2)=3v(CO2)=3×0.075molL-1min-1=0.225 molL-1min-1,故答案为:0.225 molL-1min-1;
②由图2可知,正、逆反应速率都增大,为升高温度,且逆反应速率增大更多,则反应向逆反应进行,故正反应为放热反应,故答案为:放;
③平衡时二氧化碳的浓度为0.25mol/L,则:

故500℃平衡常数K=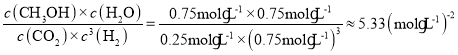 。
。
该反应正反应是放热反应,若提高温度,该反应向逆反应方向进行,达平衡时,K值减小。故答案为:5.33;减小;
④由③中计算可知,平衡时CH3OH的体积分数ω=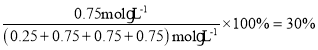 ,故答案为:30%;
,故答案为:30%;
Ⅱ(2)由盖斯定律可知,通过①×2+②+③可得3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g),则△H=-90.8kJmol-1×2-23.5kJmol-1-41.3kJmol-1=-246.4kJmol-1,故总合成反应的热化学方程式为:3H2(g)+3CO(g)
CH3OCH3(g)+CO2(g),则△H=-90.8kJmol-1×2-23.5kJmol-1-41.3kJmol-1=-246.4kJmol-1,故总合成反应的热化学方程式为:3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)△H=-246.4kJ/mol,故答案为:3H2(g)+3CO(g)
CH3OCH3(g)+CO2(g)△H=-246.4kJ/mol,故答案为:3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)△H=-246.4kJ/mol;
CH3OCH3(g)+CO2(g)△H=-246.4kJ/mol;
(3)A.由于反应放热,升高温度平衡向逆反应方向移动,CO转化率减小,A项错误;
B.催化剂不影响平衡移动,CO转化率不变,B项错误;
C.减少CO2的浓度,平衡向正反应方向移动,CO的转化率增大,C项正确;
D.增加CO的浓度,CO的转化率反而减小,D项错误;
E.分离出二甲醚,平衡向正反应方向移动,CO的转化率增大,E项正确;
故答案为CE;
(4)浓度商Qc=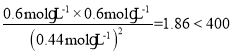 ,即Qc<K,故反应向正反应方向进行,则v(正)>v(逆)。故答案为:>。
,即Qc<K,故反应向正反应方向进行,则v(正)>v(逆)。故答案为:>。


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】(1)亚铁氰化钾是食盐中常用的抗结剂,其化学式为K4[Fe(CN)6]。
①CN-的电子式是__________;1 mol该配离子中含σ键数目为________。
②该配合物中存在的作用力类型有_________(填字母)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
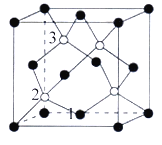
(2)磷化硼(BP)是一种超硬耐磨涂层材料,如图为其晶胞,晶胞边长为a nm。则硼原子与磷原子最近的距离为__________。 用M g·mol-1表示磷化硼的摩尔质量,NA表示阿伏加德罗常数的值,则磷化硼晶体的密度为__________g·cm-3。
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中3原子1的坐标为(1/2,1/2,0),则原子3的坐标分别为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )

①装置甲可防止铁钉生锈
②装置乙可除去乙烯中混有的乙炔
③装置丙可验证HCl气体在水中的溶解性
④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集H2、CO2、Cl2、HCl、NO2等气体
A.①⑤B.②④C.③④D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是
A. Na2CO3+2HCl=Na2CO3+CO2↑+H2O B. H2O+CO2=H2CO3
C. 2Na2O2+2H2O=4NaOH+O2↑ D. 2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为________________________________;
(2)A中的碳原子是否都处于同一平面__________________(填“是”或“不是”);
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。
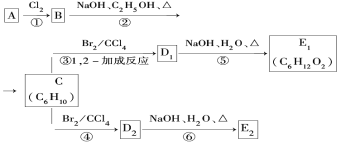
①反应②的化学方程式为____________________________________
②E2的结构简式是________________________________;
③反应④、反应⑥的反应类型依次是_________________,____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲探究CO还原CuO,设计如图所示装置(夹持装置略去)。下列说法正确的是
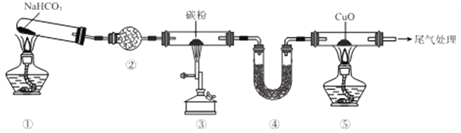
A. ②、④中均可盛装碱石灰
B. 加热的顺序为③、①、⑤
C. ①、③、⑤中均发生氧化还原反应
D. 可将尾气用导管通入到⑤的酒精灯处灼烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a-Fe(III)晶面铁原子簇是合成氨工业的一种新型高效催化剂,N2和H2在其表面首先变为活化分子,反应机理为①H2 (g)=2H(g) △H1,②N2(g)+2H(g)2(NH)(g) △H2, ③(NH)(g)+H(g)![]() (NH2)(g) △H3, ④(NH2)(g)+H(g)
(NH2)(g) △H3, ④(NH2)(g)+H(g) ![]() NH3 (g) △H4,总反应为N2 (g)+3H2(g)
NH3 (g) △H4,总反应为N2 (g)+3H2(g)![]() 2NH3 (g) △H。下列说法正确的是
2NH3 (g) △H。下列说法正确的是
A. 催化剂能够有效降低反应的活化能和改变反应的焓变
B. 增大压强和使用高效催化剂均有利于提高总反应的平衡转化率
C. 反应①和总反应均为放热反应
D. △H=3△H1+△H2+2△H3+2△H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)![]() NH2COONH4(s) △H1
NH2COONH4(s) △H1
反应Ⅱ:NH2COONH4(s)![]() CO(NH2)2(s)+H2O(g) △H2= +72.49kJ/mol
CO(NH2)2(s)+H2O(g) △H2= +72.49kJ/mol
总反应:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g) △H3= -86.98kJ/mol
CO(NH2)2(s)+H2O(g) △H3= -86.98kJ/mol
①反应Ⅰ的△H1=______________。
②一定温度下,在体积固定的密闭容器中按 n(NH3):n(CO2)=2:1 进行反应Ⅰ,下列能说明反应Ⅰ达到了平衡状态的是_______(填序号)。
A 容器内气体总压强不再变化
B NH3与CO2的转化率相等
C 容器内混合气体的密度不再变化
(2)在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应的化学平衡常数表达式为K=___________。
②该反应为____________(填“吸热”或“放热”)反应。
③某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________℃。
④在800 ℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2 mol·L-1,c(H2)为1.5 mol·L-1,c(CO)为1 mol·L-1,c(H2O)为3 mol·L-1,此时反应向________(填“正向”或“逆向”)进行。
(3)工业上从废铅蓄电池废液回收铅的过程中,常用纯碱溶液与处理后的铅膏(主要含PbSO4)发生反应:PbSO4(s)+CO32-(aq)![]() PbCO3(s)+SO42-(aq)。已知溶度积常数:Ksp(PbSO4)=1.6×10-8,Ksp(PbCO3)=7.4×10-14,则该反应的化学平衡常数K =____。
PbCO3(s)+SO42-(aq)。已知溶度积常数:Ksp(PbSO4)=1.6×10-8,Ksp(PbCO3)=7.4×10-14,则该反应的化学平衡常数K =____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是![]()
A.酸碱中和滴定时,滴定管和锥形瓶在使用前均需用待装液润洗
B.清洗碘升华实验所用试管,先用稀盐酸清洗,再用水清洗
C.实验室从海带提取单质碘的方法是:取样![]() 灼烧
灼烧![]() 溶解
溶解![]() 过滤
过滤![]() 萃取
萃取
D.配制![]() 溶液时未恢复至室温就转移并定容,所得溶液浓度偏小
溶液时未恢复至室温就转移并定容,所得溶液浓度偏小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com